Сущность - каталитическое действие
Cтраница 1
Сущность каталитического действия Н в рассмотренных реакциях заключается в том, что электрофильный реагент Н имеет свободную ( незанятую) орбиталь и избыточный положительный заряд. Свободный энергетический уровень Н может взаимодействовать с энергетическими уровнями несвязывающих орбиталей, а также с верхними заполненными молекулярными орбиталями кислорода. На свободную орбиталь Н смещается электронный заряд с несвязывающей или верхней заполненной орбитали кислорода. В результате возникает связь донорно-акцепторного типа между протоном и атомами кислорода. Распределение электронной плотности в молекуле изменяется. За счет понижения электронной плотности на связях - С-О - С - прочность их понижается, молекула поляризуется. [1]
Сущность каталитического действия Н в рассмотренных реакциях заключается в том, что электрофильный реагент Н имеет свободную ( незанятую) орбиталь и избыточный положительный заряд. Свободный энергетический уровень Н может взаимодействовать с энергетическими уровнями несвязывающих орбиталей, а также с верхними заполненными молекулярными орбиталями кислорода. На свободную орбиталь Н смещается электронный заряд с несвязывающей или верхней заполненной орбитали кислорода. В результате возникает связь донорно-акцепторного типа между протоном и атомами кислорода. Распределение электронной плотности в молекуле изменяется. За счет понижения электронной плотности на связях - С - О - С - прочность их понижается, молекула поляризуется. [2]
Сущность каталитического действия заключается в том, что ионы металлов выступают как доноры или акцепторы электронов. Химическое взаимодействие между реагирующими молекулами, координированными около центрального иона металла, облегчается благодаря поляризации молекул и понижению энергии отдельных связей. Центральный ион металла является мостиком, облегчающим электронные переходы между реагирующими молекулами. [3]
Сущность каталитического действия / / Журн. [4]
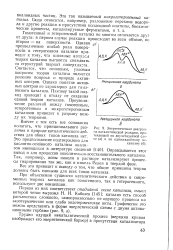 |
Энергетическая диаграмма каталитической реакции, протекающей по двухстадийной схеме ( я и по одностадийному механизму ( б. [5] |
При объяснении сущности каталитического действия в современных теориях катализа как гомогенного, так и гетерогенного, используют две концепции. [6]
 |
График Аррениуса для процессов гидратации ( / и дегидратации ( 2, протекающих по кислотно-основному ( / и окислительно-восстановительному ( / / механизму. [7] |
Основным критерием правильности той или иной концепции о сущности каталитического действия должна служить возможность использования теории для предвидения каталитического действия и научного подбора катализаторов. [8]
Эти исследования не только показывают общий путь к познанию сущности каталитического действия. [9]
Указывая на существование двух групп катализаторов, эта классификация раскрывает глубокую по своим причинным связям сущность каталитического действия. Эта сущность связана с электронной структурой вещества, с двумя типами химического взаимодействия, или химической связи, - ионным и ковалентным. [10]
Указывая на существование двух больших групп катализаторов, эта классификация впервые раскрывает самую сокровенную со времен Берцелиуса и самую глубокую по своим причинным связям сущность каталитического действия. Эта сущность связана с электронной структурой вещества, или с электрическими отношениями материи - как сказал бы Бер-целиус. Каталитическое действие и является поэтому функцией одновременно как химического состава, определяющего тип перемещающихся заряженных частиц ( а следовательно, саму принадлежность катализатора к той или другой группе), так и физического состояния, оказывающего влияние на количество и энергию перемещающихся частиц. [11]
Полученный экспериментальный материал позволил установить некоторые закономерности промотирования и формирования этих катализаторов, что является базой для дальнейшей разработки процесса синтеза углеводородов и познания сущности каталитического действия железных катализаторов. [12]
В настоящее время общепринятым является представление, согласно которому в присутствии катализаторов ( ферментов) создаются условия, при которых реакция начинает протекать как бы в обход энергетического барьера. Другими словами, сущность каталитического действия сводится с энергетической точки зрения к снижению энергии активации. В присутствии катализатора реакция становится возможной на новом, более низком энергетическом уровне, вследствие чего при данных температурных условиях способным к реакции оказывается больший процент молекул. Отсюда понятно, почему скорость реакции в присутствии катализатора резко возрастает. [13]
Это отчетливо вытекает из того, что химическая кинетика до сих пор бессильна предсказать скорость даже самых простых, некаталитических реакций. Всякий же каталитический процесс всегда сложнее, так как в этом случае в состав активного комплекса наряду с реагирующими веществами обязательно входит и катализатор. Тем не менее мы можем оптимистично оценивать перспективы развития теории предвидения каталитического действия. Основанием для этого является ясность, достигнутая теорией в трактовке сущности каталитического действия, а также быстрый прогресс методов прямого экспериментального изучения промежуточного поверхностного взаимодействия реагирующих веществ с катализатором. Интенсивное накопление этих экспериментальных данных позволит создавать обобщения, первоначально узкие, но постепенно охватывающие все более широкие области гетерогенного катализа, и предсказывать наиболее плодотворные направления поисков новых катализаторов. [14]
Реакции восстановления, гидрирования, окисления, гидратации ненасыщенных соединений, изомеризации, полимеризации и многие другие в промышленных условиях осуществляются в растворах в присутствии комплексных катализаторов. По типу применяемых катализаторов эти процессы иногда объединяют в группу координационного катализа. В качестве катализаторов в таких процессах применяются комплексные соединения катионов переходных металлов. Сюда относятся металлы VIII группы Fe, Co, Ni, Ru, Rh, Pd, Os, IT, Pi, а также Си, Ag, Hg, Cr и Мп. Сущность каталитического действия заключается в том, что ионы металлов с d - электронной конфигурацией d6 - d10 могут взаимодействовать с другими молекулами, выступая как акцепторы электронов, принимая электроны на свободные d - орбитали, и как доноры электронов. Донорно-акцепторное взаимодействие, обусловленное переходом электронов с я-орбитали этилена, уменьшает электронную плотность между атомами углерода и, следовательно, уменьшает энергию связи СС. [15]
Страницы: 1 2