Внутренняя сфера - комплекс
Cтраница 2
Лабильность внутренней сферы комплексов зависит не только от природы центрального атома, но и от природы внутрисферных лигандов. Например, скорость образования дигидроксодимеров типа [ PtaL4 ( OH) 2 ] a из комплексов fPt L2 ( HaO) OH ] в значительной мере должна зависеть от транс-и цисвлияния лигандов L. Известно, что для соединений платиновых металлов проявление взаимного влияния лигандов особенно характерно. [16]
Диссоциация внутренней сферы комплекса, как всякого слабого электролита, процесс обратимый. [17]
Диссоциация внутренней сферы комплекса, как всякого слабого электролита, - процесс обратимый. [18]
Пространственная структура внутренней сферы комплекса определяется, в основном, координационным числом и стремлением к достижению максимальной компактности ( плотности) упаковки частиц. При координационных числах 4 и ниже значительную роль для относительной устойчивости того или иного пространственного расположения играют индивидуальные особенности комплексообразователя и аддендов. [19]
Центральный элемент внутренней сферы комплекса, вокруг которого группируются ионы или молекулы, называется комплексо-образователем или ядром комплекса. Роль комплексообразовате-лей чаще всего выполняют катионы переходных металлов, реже анионы или нейтральные атомы. Ионы или молекулы, координирующиеся возле центрального атома во внутренней сфере, называются лигандами. [20]
 |
Октаэдр ( а Опыт показывает, однако, что для мно. [21] |
Пространственная структура внутренней сферы комплекса определяется, в основном, координационным числом и стремлением к достижению максимальной компактности ( плотности) упаковки частиц. При координационных числах 4 и ниже значительную роль для относительной устойчивости того или иного пространственного расположения играют индивидуальные особенности комплексообразователя и лигандов. [22]
Если во внутреннюю сферу комплекса входит молекула, характеризующаяся высокой трансактивностью, напр. [23]
Они образуют внутреннюю сферу комплекса. Кроме внутренней сферы [ в квадратных скобках выражения ( 32) ] в комплексных соединениях существует и внешняя сфера, в которой находится ион натрия. [24]
Замена во внутренней сфере комплексов одних аддендов другими часто сопровождается изменением окраски раствора. Так, комплексное соединение [ Сг ( ОН2) 6 ] С13 имеет фиолетовую окраску, [ Сг ( ОН2) 5С1 ] С12 - Н2О - светлозеленую и [ Сг ( ОН2) 4С12 ] С1 - 2Н2О - темнозеленую. Комплексная соль [ Со ( NH3) 6 ] C13 имеет оранжево-желтый цвет, [ Со ( NH. [25]
Замена во внутренней сфере комплексов одних аддендов другими часто сопровождается изменением окраски раствора. [26]
Замена во внутренней сфере комплекса одного лиганда другим приводит к изменению свойств соединения. В частности, это сказывается на его окраске. [27]
Поскольку во внутренней сфере комплекса содержится хлор или бром, все эти продукты окрашены в различные оттенки желтого цвета. [28]
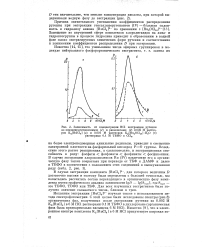 |
Зависимость от концентрации НС1 экстракции рутения из свежеприготовленных ( 1 и равновесных ( 2 М растворов K2 [ RuCle ] ( а и М растворов K4 [ Ru2OCl10 ] - H20 ( б растворами М ТБФО в СС14. [29] |
Замещение во внутренней сфере комплексов хлоролигандов на аква - и гидроксогрушш в процессе гидролиза приводит к образованию в водной фазе плохо экстрагируемых химических форм рутения и соответственно к понижению коэффициентов распределения D при экстракции. [30]
Страницы: 1 2 3 4