Схема - молекула
Cтраница 1
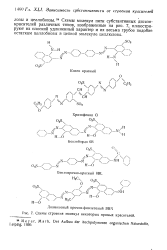 |
Схемы строения молекул некоторых прямых красителей. [1] |
Схемы молекул пяти субстантивных дисазо-красителей различных типов, изображенные на рис. 7, иллюстрируют их плоский удлиненный характер и их весьма грубое подобие остаткам целлобиозы в цепной молекуле целлюлозы. [2]
 |
Схематическое представление ls - орбитали в / С-оболочке атома углерода ( слева и четырех тетраэдрических орбиталей L-оболочки ( справа. [3] |
Схема молекулы циклопропана СзН6 показывающая деформацию связей углерод - углерод. [4]
Схема молекулы этилена приведена на рис. 3, там же указана нумерация атомов. [5]
Нарисуйте схемы молекул этилена и пропилена с обозначением направления осей о-связей и значений валентных углов. Какие виды а-связей имеются в молекуле пропилена. [6]
Нарисуйте схему молекулы пропилена с обозначением направления осей а-связей и величины валентных углов. [7]
По этой схеме молекулы воды проникают в ближайшую координационную сферу атома кремния, находящегося в цет тре кислородного тетраэдра, и неподеленные электронные пары атома кислорода молекулы воды взаимодействуют с вакантными d - орбитами атома кремния. [8]
По этой схеме молекулы воды проникают в ближайшую координационную сферу атома кремния, находящегося в центре кислородного тетраэдра, и неподеленные электронные пары атома кислорода молекулы воды взаимодействуют с вакантными d - орбитами атома кремния. [9]
В приведенной ниже схеме молекулы СаНь, все атомы углерода которых находятся в 5р2 - гибридных состояниях, классифицируются согласно их топологии. [10]
Приведенная на этом рисунке схема молекулы фтористого водорода является, однако, лишь грубым, приближением. Из приведенной схемы видно, что вандерваальсовский радиус является как бы внешним радиусом, имеющим большое значение в кинетической теории. Понятие о внешнем радиусе вытекает из поведения реальных газов. [11]
 |
Схема строения макромолекулы полиэтилена низкого ( а и высокого ( б давления. [12] |
На рис. 17 показана схема молекулы полиэтилена высокого давления и полиэтилена, получаемого под низким давлением. [13]
В табл. 4.4 также представлена схема МО молекулы оксида углерода СО. Здесь на МО переходят шесть электронов атома кислорода и четыре электрона атома углерода. Энергии электронов ( например, 2р - электронов) соединяющихся атомов неодинаковы: заряд ядра атома кислорода выше, чем заряд ядра атома углерода, так что 2р - электроны в атоме кислорода сильнее притягиваются ядром. Поэтому на рис. 4.22 расположение 2р - АО кислорода должно быть ниже уровня расположения 2р - АО углерода. Наличие в молекуле СО избытка шести связывающих электронов над разрыхляющими отвечает, как и в молекуле азота, образованию тройной связи. [14]
 |
Ковалентные и эффективные радиусы атоЫОв и углы между связями. [15] |
Страницы: 1 2