Схема - терм
Cтраница 2
В спектре VI в схему термов уложено свыше 2000 линий. Ионы Сг И, Мп HI, Fe IV, Со V и Ni VII имеют, как и VI, набор секстетных, квартетных и дублетных термов, но нормальным у всех у них является терм 3d56S, а не терм 3d34s24F, как у ванадия. На графиках Мозелея, приведенных на рис. 145, характерно пересечение линией терма 3d56S линий остальных термов. [16]
Рассмотрим в качестве примера схему термов N. [17]
В основном аналогичный вид имеют схемы термов Si, Ge, Sn, Pb. [18]
На рисунках 160 и 161 мы приводим схемы термов и линий Не I. В спектре Не I интеркомбинационный запрет строго соблюдается. [19]
На рис. 1 1 уровни энергии ( схема термов) представлены графически. Справа на ординате нулевой точкой служит наименьшее из возможных значений энергии связи, при котором электрон еще остается связанным; оно называется также границей серии. Максимальная энергия связи ( 13 59 эВ) равнозначна энергии ионизации атома водорода, которая может быть определена также при помощи других методов. [20]
Схема термов 21 Sell позволяет перейти к схеме термов нейтрального Scl. При этом терм 2D будет единственно возможным, соответствующим конфигурации 3d 4s2, так как два 45-электрона по принципу Паули должны иметь компенсированные спиновые моменты. [21]
Их называют термами, а соответствующие диаграммы - схемами термов. [22]
После того как проведен анализ молекулярного спектра и получена схема термов, задача сводится к определению процентной доли молекул, которые будут находиться в каждом данном квантовом состоянии при каждой данной температуре. [23]
Поскольку такие термы не реализуются, их исключение из схемы термов должно быть оправдано теоретически. Причину мы видим в том, что маятникообразные орбиты проходят через ядро, и электрон в своем движении по ним сталкивался бы с ядром, что, конечно невозможно. [24]
Значения величин v, Em, gm находятся из схемы термов элементов, излучение которого регистрируется. [25]
Поэтому каждому значению азимутального квантового числа соответствуют три уровня и схема термов ортогелия образует систему триплетов. Но и здесь, так же как в рассмотренных выше дублетных спектрах ( § 1), s - терм не расщепляется. В щелочноземельных металлах ( Be, Mg, Ca, Sr, Ва), которые, подобно гелию, имеют по два внешних электрона, три-плетный характер спектров легко наблюдается. Однако спектр гелия имеет особенность: практически он состоит из дублетов, так как уровни Р4 и Р2 почти совпадают. [26]
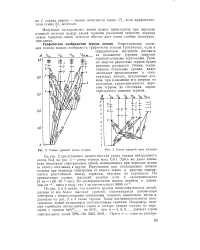 |
Схема уровней атома натрия.| Схема уровней иона кальция. [27] |
На рис. 2 представлена энергетическая схема термов нейтрального атома Nal, та рис. 3 - схема термов иона Call. Здесь же даны длины волн некоторых спектральных линий, возникающих при переходе атома из одного состояния в другое. Излучаемая или поглощаемая атомом энергия при переходе электронов от одного терма к другому определяется расстоянием между термами, взятыми по вертикали. [28]
Мы приводим на рис. 4, в качестве примера, схему возможных энергетических состояний атомов водорода или, как ее называют схему термов. [29]
 |
Эмпирические условные радиусы ионов и атомов ( А. [30] |
Страницы: 1 2 3