Схема - энергетические уровни
Cтраница 3
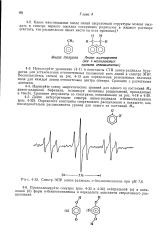 |
Спектр ЭПР анион-радикала о-бензосемихинона при рН 7 6. [31] |
Нарисуйте схему энергетических уровней для одного из состояний Ms: Энион-радикала бифенила, используя величины расщеплений, приведенные в тексте. [32]
Рассмотрим схему энергетических уровней нейтральных атомов, начиная с более простых случаев. На рис. 51 приведен ход энергетических термов нейтральных атомов, который отвечает постепенному нарастанию ядерного заряда. При сравнении рис. 51 с графиком радиусов максимальной плотности, приведенном на рис. 24, видна ярко выраженная антибатность. При движении от Н до Мп уменьшению радиусов орбиталей отвечает увеличение энергетических характеристик. [33]
На схеме энергетических уровней, за последней квантовой орбитой п оо простирается заштрихованная область непрерывного энергетического спектра. Это соответствует тому, что электроны, вырванные из атома водорода, обладают кинетической энергией, равной разности между энергией, необходимой для ионизации, и энергией падающих электронов. Электроны, находящиеся вне агома водорода, не подчиняются квантовым условиям, так как их движение не периодично. Кинетическая энергия этих электронов может иметь любое значение. Если электрон, находящийся вблизи иона водорода, переходит на одну из его орбит, то система излучает энергию. Если первоначальная кинетическая энергия электрона равна нулю и он падает на орбиту / 2 2, система излучает некоторое количество энергии, соответствующее предельной линии серии Бальмера. Если первоначальная кинетическая энергия электрона больше нуля и он падает на орбиту / / 2, то система будет излучать большее количество энергии. [34]
О схеме энергетических уровней любого кристалла часто говорят как о его зонной структуре, или структуре полос. Каждлао из функций (2.19), заданных в точках первой зоны Бриллюэна, можно представить в виде кривой, причем любой из кривых отвечает на оси е своя полоса. В частном случае, когда т 1 ( простая цепочка), вековое уравнение (2.18) сводится к соотношению (2.11), которое определяет единственную ветвь закона дисперсии с соответствующей ей одной полосой. [35]
I показана схема энергетических уровней для золота в германии, предложенная на основе приведенных фактов. [36]
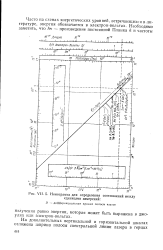 |
Номограмма для определения соотношений между единицами измерений. [37] |
Часто на схемах энергетических уровней, встречающихся в литературе, энергия обозначается в электрон-вольтах. [38]
Таким образом, схема энергетических уровней л - МО молекулы этилена практически не отличается от схемы сг - МО молекулы водорода. [39]
На основе сопоставления схем энергетических уровней рассмотренных КРЭЯ оценить положение локальных уровней относительно зон совершенного кристалла, а также другие характеристики ЛЦ с помощью полученных одноэлектронных функций локальных уровней. [40]
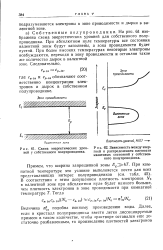 |
Схема энергетических уровней у собственного полупроводника.| Зависимость между энергией и распределением плотности квантовых состояний у собственного полупроводника. [41] |
На рис. 61 изображена схема энергетических уровней для собственного полупроводника. При абсолютном нуле температуры все состояния валентной зоны будут заполнены, а зона проводимости будет пустой. При более высоких температурах некоторые электроны возбуждаются, переходя в зону проводимости и оставляя такое же количество дырок в валентной зоне. [42]
 |
Адсорбция кислорода на окиси цинка. [43] |
На рис. 1 представлена схема энергетических уровней в предполагаемой зонной модели окиси цинка. Валентная зона и зона проводимости разделены запрещенной областью. В последней указаны два уровня, соответствующие переходу двух электронов на междуузелышй цинк. [44]
На рис. 18 показана схема энергетических уровней и переходов между ними у атома лития. В отличие от схемы уровней водорода ( рис. 16), серии уровней s, p, d, f изображены раздельно, поскольку их энергии не совпадают между собой из-за различия квантовых дефектов. Уровни энергии щелочных металлов имеют мультиплетность х2 и поэтому называются дублетными. [45]
Страницы: 1 2 3 4