Схема - энергетические уровни - атом - водород
Cтраница 1
 |
Схема энергетических уровней. [1] |
Схема энергетических уровней атома водорода, построенная на основании спектральных данных, изображена. [2]
Схема энергетических уровней атома водорода, построенная на основании спектральных данных, изображена на рис. 360 в виде ряда параллельных линий. Поэтому расстояния между уровнями выражают в некотором масштаба частоты спектральных линий водорода. [3]
Схема энергетических уровней атома водорода, построенная на основании спектральных данных, изображена на рис. 360 в виде ряда параллельных линий. Поэтому расстояния между уровнями выражают в некотором масштабе частоты спектральных линий водорода. [4]
Схема энергетических уровней атома водорода, построенная на основании спектральных данных, изображена на рис. 354 в виде ряда параллельных линий. Поэтому величины этих расстояний выражают также в некотором масштабе частоты спектральных линий водорода. [6]
Схема энергетических уровней атома водорода может быть использована при рассмотрении водородоподобных атомов; нужно только изменить шкалу, так как энергетические термы, если пренебречь релятивистскими членами, отличаются лишь коэ-фнциентом. [7]
Рассмотренная выше схема энергетических уровней атома водорода является простейшей. Чем больше электронов имеет атом, тем сложнее схема его энергетических уровней и спектр. Так, спектр железа состоит из нескольких тысяч линий. [8]
Рассмотренная выше 7ff схема энергетических уровней атома водорода является простейшей. Чем больше электронов имеет атом, тем сложнее схема его энергетических уровней и спектр. Так, спектр железа состоит из нескольких тысяч линий. [9]
Па рис. 38.3 приведена схема энергетических уровней атома водорода. Стрелками указаны переходы, соответствующие излучению различных серий спектральных линии. Ej Правило частот не могло быть навеяно никакими эмпирическими формулами и явилось гениальной догадкой Бора. Бору рассчитать спектр атома водорода и других изоэлектронных водороду систем, а также теоретически вычислить соответствующие им значения постоянной Ридберга, находящиеся в хорошем согласии с опытом. [10]
На рис. 13.3 приведена схема энергетических уровней атома водорода. Стрелками указаны переходы, соответствующие излучению различных серий спектральных линий. [11]
Подставив в это соотношение значение R1, получим для потенциала ионизации атома водорода из нормального состояния ( п) величину ф 13 53 в. На рис. 13.3 приведена схема энергетических уровней атома водорода. Стрелками указаны переходы, соответствующие излучению различных серий спектральных линий. [12]
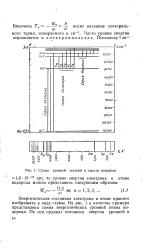 |
Схема уровней энергий и спектр водорода. [13] |
Энергетические состояния электрона в атоме принято изображать в виде схемы. На рис. 1 в качестве примера представлена схема энергетических уровней атома водорода. [14]
С этого момента речь идет об атоме водорода. Классически он представляет собой простейший атом. Как выясняется, схема энергетических уровней атома водорода поддается легкому описанию в отношении численных значений, чем он отличается от атома ртути. [15]
Страницы: 1 2
