Ионная схема
Cтраница 2
В ионно-электронном методе подбор коэффициентов производится в несколько стадий. Сначала составляют общую ионную схему данной реакции, определяют восстановитель и окислитель. Затем составляют частные ионно-электронные уравнения отдельно для реакции окисления и реакции восстановления. После этого частные уравнения суммируют, находят общий наибольший делитель для числа отдаваемых и принимаемых электронов и получают полное ионно-электронное уравнение. [16]
В ионно-электронном методе подбор коэффициентов производится в несколько стадий. Сначала составляют общую ионную схему данной реакции, определяют восстановитель и окислитель. Затем составляют частные ионно-электронные уравнения отдельно для реакции окисления и реакции восстановления. После этого частные уравнения суммируют, находят наименьшее общее кратное для числа отдаваемых и принимаемых электронов и получают полное ионно-электронное уравнение. [17]
Этот метод применяют только для окислительно-восстановительных процессов в растворах электролитов. Начинают с составления ионной схемы реакции, руководствуясь общими правилами составления ионных уравнений: записывают сильные электролиты в виде ионов, слаб ые электролиты, неэлектролиты, осадки и газы - в виде молекул. Ионы, не претерпевающие изменения, в схему не включаются. [18]
Ионно-электронный метод составления уравнений окислительно-восстановительных реакций применяется для ионных окислительно-восстановительных процессов и основан на составлении частных уравнений реакций восстановления ионов ( молекул) окислителя и окисления ионов ( молекул) - восстановителя с последующим суммированием их в общее уравнение. Для этого необходимо составить ионную схему реакции. Не изменяющиеся в результате реакции ионы в ионную схему не включаются. [19]
Ионно-электронный метод составления уравнений окислительно-восстановительных реакций применяется для ионных окислительно-восстановительных процессов и основан на составлении частных уравнений реакций восстановления ионов ( молекул) - окислителя и окисления ионов ( молекул) - восстановителя с последующим суммированием их в общее уравнение. Для этого необходимо составить ионную схему реакции. Не изменяющиеся в результате реакции ионы в ионную схему не включаются. [20]
Йонно-электронный метод составления у эавнений окислительно-восстановительных реакций применяется для и энных окислительно-восстановительных процессов и основан на составлении частных уравнений реакций восстановления ионов ( молекул) - окислителя и окисления ионов ( молекул) - восстановителя с последующим суммированием их в общее уравнение. Для этого необходимо составить ионную схему реакции. Не изменяющиеся в результате реакции ионы в ионную схему не включаются. [21]
Напишите реакции взаимодействия между: а) нитратом марганца и диоксидом свинца в присутствии азотной кислоты; при этом нитрат марганца окисляется до марганцевой кислоты; б) иодидом водорода и азотистой кислотой, при этом азотистая кислота восстанавливается до оксида азота; в) медью и концентрированной азотной кислотой. Для всех реакций составьте электронно - ионные схемы и подберите коэффициенты. [22]
При написании ионных уравнений сильные электролиты записывают в виде ионов, а неэлектролиты, слабые электролиты, газы и осадки - в виде молекул. Не изменяющиеся в результате реакции ионы в ионную схему не включаются. [23]
Ионно-электронный метод составления уравнений окислительно-восстановительных реакций / применяется для ионных окислительно-восстановительных процессов и основан на составлении частных уравнений реакций восстановления иона ( молекулы) - окислителя и окисления иона ( молекулы) - восстановителя с последующим суммированием их в общее уравнение. Не изменяющиеся в результате реакции ионы в ионную схему не включаются. [24]
Как видно из табл. 59, учет реальной ионности химической связи в кристаллах позволил затметно увеличить точность вычисления мольных рефракций. Как и в случае молекул, среднее отклонение от средней ошибки в новом методе значительно меньше, чем в классических методиках: в ионной схеме ДЛ. [25]
На основании проведенных исследований можно считать, что крем-иийорганические соединения ( главным образом кремнеуглеводороды) очень инертны к ионным инициаторам полимеризации и несколько активнее к радикальным инициаторам. Так, например, Каназаши ( 242 ] было установлено, что в случае триметилвинилсилана полимеризация по радикальной схеме приводит к образованию тримера, а полимеризация по ионной схеме ( А1С13) не имет места вообще. [26]
Напротив, сила кислородных кислот хлора возрастает с увеличением его степени окисленности. Ионная схема моле - хлорная. [27]
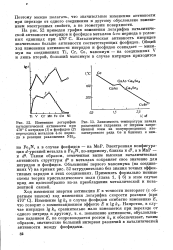
Таким образом, отмеченная выше высокая каталитическая активность структуры d6 в металлах сохраняет свое значение для нитридов и фосфидов. Объяснение первого максимума ( на соединениях V) на кривых рис. 52 затруднительно без знания точных эффективных зарядов в этих соединениях. Применять формально ионные схемы теории кристаллического поля ( глава 1, § 6) в этом случае вряд ли целесообразно из-за преобладания металлической и кова-лентной связей. [29]
Составляя уравнения окислительно-восстановительных реакций в растворах электролитов, применяют также электронно-ионный метод составления уравнений. Основное отличие этого метода от рассмотренного ранее сводится к следующему. На основе ионной схемы реакции составляют электронно-ионные уравнения для процессов восстановления и окисления. Обращают внимание на то, чтобы ал-гебраическая сумма зарядов в обеих частях каждого уравнения была одинаковой. После этого ионные уравнения суммируют, предварительно умножив на коэффициенты при окислителе и восстановителе, найденные обычным путем. [30]
Страницы: 1 2 3