Таблица - растворимость
Cтраница 3
Рассчитывают по таблице растворимости хлористого бария какая часть соли выпадает в осадок при охлаждении от 95 С ( температуры раствора на кипящей бане) до комнатной температуры. [31]
Познакомиться с таблицей растворимости квасцов, хлористого натрия, уксуснокислого кальция и начертить кривые их растворимости, отложив по оси абсцисс температуру, а по оси ординат концентрацию насыщенного раствора. [32]
Решение, По таблице растворимости ( табл. 6) находим растворимость нитрата калия при 80 и 20 С. [33]
Выберите, пользуясь таблицами растворимости или кривыми растворимости те вещества, растворимость которых зависит заметно от температуры, например при повышении температуры от 0 до 100 С возрастает не менее чем в 3 раза, и перекристаллизуйте их. Ниже очистка перекристаллизацией будет описана на примере медного купороса. [34]
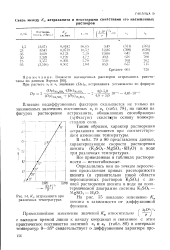 |
Kv астраханита при различных температурах. [35] |
Все приведенные в таблицах растворимости - метастабишьные. [36]
По этой ф-ле составлены таблицы растворимости С. III); при 0 в 100 г воды растворяется 179 г С. [37]
По этой ф-ле составлены таблицы растворимости С. [38]
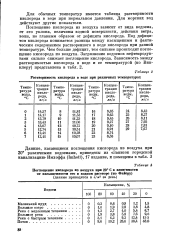 |
Растворимость кислорода в воде при различных температурах. [39] |
Для обычных температур имеется таблица растворимости кислорода в воде при нормальном давлении. Для морских вод действуют другие показатели. [40]
Уравнение реакции напишите самостоятельно, пользуясь таблицей растворимости оснований и солей. [41]
Пары подобных веществ можно легко найти в таблице растворимости. [42]
Растворимость в воде важнейших солей указана в таблице растворимости. [43]
Сульфид марганца, как это можно установить по таблицам растворимости, практически не растворяется в воде, значит, формулу его надо писать в виде MnS, так как количество ионов Мп2 и S2 -, находящихся в насыщенном водном растворе MnS, ничтожно. Соляная кислота принадлежит к числу сильных, полностью диссоциированных, значит, в растворе практически нет молекул НС1, а находятся только Н и С1 - ионы. [44]
Сульфид марганца, как это можно установить по таблицам растворимости, практически не растворяется в воде, значит, формулу его надо писать в виде MnS, так как количество ионов Мп2 и S2 -, находящихся в насыщенном водном растворе MnS, ничтожно. Соляная кислота принадлежит к числу сильных, полностью диссоциированных, значит, в растворе практически нет молекул НС1, а находятся только Н и С1 - ионы. Из этих ионов С1 - ионы никакой роли играть не могут, так как с ионами Мп2 они могут дать лишь. [45]
Страницы: 1 2 3 4