Пятихлористый тантал
Cтраница 1
Пятихлористый тантал, невидимому, так же активен, как хлористый алюминий, а хлористый цирконий одинаково или даже более активен, чем хлористый алюминий. [1]
Пятихлористый тантал взаимодействует с реактивами Гринья-ра, давая окрашенные растворы, изменяющиеся под действием воздуха и воды [96]; кроме этого больше ничего не известно относительно возможных алкильных или арильных производных. [2]
Дегалогенирование пятихлористого тантала и последующая обработка разбавленной кислотой приводят к образованию Та6С114 - 7Н2О, в котором только два атома хлора немедленно осаждаются раствором нитрата серебра. [3]
В литературе описан метод получения тетрахлорида тантала [1], основанный на восстановлении пятихлористого тантала металлическим алюминием. Для проведения этой реакции авторы помещали раздельно алюминиевую фольгу и избыток пятихлористого тантала в стеклянную трубку с тремя температурными зонами ( 400, 230, 200), вакуумирова-ли до остаточного давления 1 10 - 4 мм и нагревали в течение 70 часов. [4]
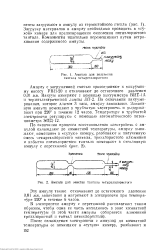 |
Ампула для получения тантала четыреххлористого.| Ампула для очистки тантала четыреххлористого. [5] |
Загрузку материалов в ампулу необходимо проводить в сухой камере для предотвращения окисления пятихлористого тантала. Компоненты тщательно перемешивают путем встряхивания содержимого ампулы. [6]
 |
Кривые вымывания ниобия. [7] |
Пятнхлористый ниобий легче восстанавливается водородом ( или металлами, например алюминием) до низших хлоридов, чем пятихлористый тантал. Это использовано для разделения тантала и ниобия. [8]
К недостаткам метода следует отнести трудность его осуществления как непрерывного и необходимость повторения операций с конденсатом для получения чистого пятихлористого тантала. [9]
Гайк и Гинтерауэр действительно получили сульфат тантала состава Taz ( S04) 5 при добавлении серного ангидрида к раствору пятихлористого тантала в хлористом сульфуриле. [10]
Для всех смесей хлористых солей Nb и А1 парциальное давление NbCl5 изменяется согласно закону Рауля. Пятихлористый тантал в сплавах с А1С13 ведет себя также, как и NbCl5, образуя ограниченный твердый раствор. Давление паров над сплавами системы FeCl3 - A1C13 при постоянной температуре является функцией их состава: с уменьшением в сплаве содержания А1С13 давление его паров понижается по закону Рауля. [11]
Определение давления паров смесей хлоридов А1 и Та показало, что парциальные давления паров хлоридов с изменением состава смеси изменяются с небольшим отклонением от закона Рауля. Пятихлористый тантал ТаС15, подобно NbCl5, образует с А1С13 растворы. На основании тензиметрических исследований тройных систем NbCl5 - А1С13 - NaCl и ТаС15 - А1С13 - NaCl в интервале температур 140 - 500 С установлено, что в случае избытка в смеси хлорида Na хлористый алюминий в газовой фазе и в отгонке не обнаружен. [13]
В литературе описан метод получения тетрахлорида тантала [1], основанный на восстановлении пятихлористого тантала металлическим алюминием. Для проведения этой реакции авторы помещали раздельно алюминиевую фольгу и избыток пятихлористого тантала в стеклянную трубку с тремя температурными зонами ( 400, 230, 200), вакуумирова-ли до остаточного давления 1 10 - 4 мм и нагревали в течение 70 часов. [14]
Результаты изучения внутренних разрезов систем ( рис. 23 и 24) указывают на наличие двух полей первичной кристаллизации на поверхности ликвидуса каждой системы. Эти поля первичной кристаллизации соответствуют первичному выделению твердых растворов хлорного железа с хлористым алюминием и ограниченных твердых растворов на основе пятихлористого тантала или пятихлористого ниобия. Максимальной температурой плавления обладают сплавы, прилегающие к вершине хлорного железа, а минимальной температурой плавления - сплавы, прилегающие к линиям вторичных выделений. Область первичной кристаллизации ограниченных твердых растворов на основе пятихлористого тантала или пятихлористого ниобия мала по сравнению с областью твердых растворов хлорного железа с хлористым алюминием. [15]
Страницы: 1 2
