Изменение - равновесное давление
Cтраница 1
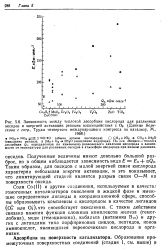
Изменение равновесного давления вследствие уменьшения растворимости компонента в водном растворе ( например, при высаливании) может, разумеется, вызываться и присутствием в пробе других соединений ( см. разд. На это обстоятельство необходимо обращать внимание, в частности, при анализе алкогольных напитков, для которых характерны большие колебания концентраций разных веществ от пробы к пробе, что может приводить к ошибкам при количественной интерпретации результатов анализа. Так, например, большие концентрации этанола влияют на растворимость ( и, следовательно, на давление паров) других веществ, присутствующих в меньших концентрациях. На рис. 30 показано влияние этанола на результаты определения амиловых спиртов и сложных эфиров. [1]
Исследуют изменение равновесного давления одного из компонентов как функцию состава нестехиометрического соединения. Применяемые соотношения подобны рассмотренным при взаимосвязи электронной проводимости или коэффициентов диффузии с парциальным давлением газа более летучего компонента. [2]
 |
Изобара адсорбции водорода на окиси цинка при давлении 760 мм. 1 - после 1000 мин.. [3] |
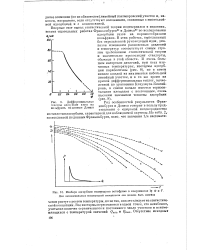
Кривая, выражающая изменение равновесного давления с изменением температуры при постоянном количестве адсорбированного газа, называется изосте-рой адсорбции. На рис. 15 изображены в виде изо-стер опытные данные Титова [21] по адсорбции аммиака на древесном угле. На рисунках 3, 11 и 15 представлены одни и те же экспериментальные данные в форме изотерм, изобар и изостер. [4]
 |
Коэффициенты уравнения Дубинина М.М. для изотерм сорбции ВРз на. [5] |
В последнем способе регулирование потока нейтронов достигается изменением равновесного давления в 10ВРз канале при нагреве или охлаждении угля. Достоинство такого способа состоит в том, что он позволяет профилировать нейтронный поток по высоте активной зоны реактора. По мнению авторов [46] такое выгорание может быть полностью скомпенсировано соответствующим уменьшением температуры адсорбента в регуляторе или увеличением ее в питателе, что приведет к дополнительной адсорбции трехфтористого бора в регуляторе. Поскольку образующиеся при этом газы распределяются по всему объему системы регулирования, который в несколько раз превышает объем угля в регуляторе, где происходит реакция, то давление в системе будет во столько же раз меньше. Учитывая это, авторы [46] до ресурса 1000 часов не рекомендуют принимать каких-либо специальных мер для компенсации прироста давления в регулирующем устройстве. [6]
Предельная концентрация CuFeO2 в закиси меди, рассчитанная из изменения равновесного давления кислорода ( 83, 84 ] для реакции ( 11 4) при переходе от системы СиО к Си-Fe - О, составляет 6 мол. [7]
По оси абсцисс - теплота десорбции QO, определенная по изменению равновесного давления кислорода в зависимости от температуры для различных оксидов в атмосфере кислорода при низком давлении. [9]
В этих работах, выполненных без определенной руководящей идеи, диапазон изменения равновесных давлений и температур соответствует самым строгим требованиям статистической теории и значительно превосходит стандарты, обычные в этой области. [11]
Из опыта известно, что в процессах плавления, испарения и сублимации изменение равновесного давления с температурой не зависит от полного объема системы. [12]
Опытные данные, подтверждающие изотерму Лэнгмюра, обычно получались в небольшом интервале изменения равновесных давлений, как правило, не более одного-двух порядков. Проведение адсорбционных измерений в достаточно большом интервале изменений равновесных давлений ( на шесть-семь порядков) показало, что часто более применимой оказывается степенная изотерма Фрейндлиха. [13]
Опытные данные, подтверждавшие уравнение Лэнгмюра, обычно получались в небольшом интервале изменения равновесных давлений, как правило - не более одного-двух порядков. [14]
Действительно, как показано в [17], адсорбция азота на вольфраме и железе по данным [532 ] и [533 ] в интервале изменений равновесных давлений на 2 - 6 порядков описывается в равной степени уравнениями обеих изотерм. [15]
Страницы: 1 2 3