Наибольшее изменение - величина
Cтраница 2
 |
Типичные кривые потенциометрического титрования. [16] |
Пусть имеется раствор НС1, который титруют раствором NaOH. Полагая, что концентрации равны активностям и пренебрегая эффектом электрострикции, можно определить изменение концентрации водородных ионов, величины рН и ( по формуле Нернста) потенциала индикаторного электрода в ходе титрования. Из рис. 30 следует, что наибольшее изменение величины потенциала индикаторного электрода наблюдается вблизи точки эквивалентности. [17]
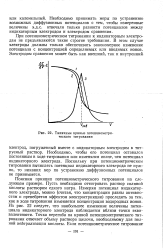 |
Типичные кривые потенциометри-ческого титрования. [18] |
Поясним принцип потенциометрического титрования на следующем примере. Пусть необходимо оттитровать раствор соляной кислоты раствором едкого натра. Измеряя потенциал индикаторного электрода, можно ( считая, что концентрации равны активностям и пренебрегая эффектом электрострикции) проследить за тем, как в ходе титрования изменяется концентрация водородных ионов. Из рис. 22 следует, что наибольшее изменение величины потенциала индикаторного электрода наблюдается вблизи точки эквивалентности. Точка перегиба на кривой потенциометрического титрования отвечает объему раствора щелочи, необходимому для полной нейтрализации кислоты. [19]
Страницы: 1 2