Температура - диссоциация
Cтраница 1
Температура диссоциации СаСО3 при парциальном давлении С02, равном 0 1 МПа, по данным различных исследователей, колеблется от 1085 до 1201 К. Причинами этого являются различная дисперсность порошка карбонатной породы и неодинаковые примеси в природных материалах. С уменьшением размера частиц СаСОз скорость их разложения возрастает. [1]
Температуры диссоциации несколько различны для доломитов разных месторождений и уменьшаются с увеличением содержания в минерале примесей. Мелкокристаллические доломиты начинают диссоциировать при более низкой температуре. [2]
Температура диссоциации карбидов или начала диффузионного процесса является понятием условным. Под этой температурой следует подразумевать такую, при которой в данной среде наступает более или менее быстрая реакция. [3]
Температура диссоциации доломита составляет 730 С, известняка - 910 С, а магнезита - 640 С. [4]
Температура диссоциации углекислого железа, по данным многих авторов, колеблется в пределах 360 - 450 С, а для углекислого марганца начало разложения относится к 300 С. Что касается устойчивости солей сернистых соединений, в частности сульфидов железа и марганца, то температура разложения их выше 1200 С. [5]
Температуры диссоциации гидроокисей магния и кальция были определены при давлениях в 4 1; 5 8; 8 4; 10 3 и 15 1 атпм. Для согласования с предыдущими определениями IgP относится к давлению, выраженному в миллиметрах ртутного столба. [6]
Температура диссоциации двухатомной молекулы зависит от ее энергии диссоциации, которая равна энергии образования этой молекулы из атомов. [7]
Температура диссоциации карбидов твердого сплава приобретает важное значение для химической стойкости инструмента. Очевидно, эта температура зависит от прочности связи атомов в карбиде. [8]
Температура диссоциации чистого карбоната кальция составляет 880 С. [9]
Температура диссоциации различных солей аммония зависит от силы соответствующей кислоты. Карбонат аммония ( МН4) 2СО3 - соль слабой кислоты - сильно пахнет аммиаком и на воздухе через некоторое время улетучивается. Фактически при комнатной температуре давление пара аммиака над солью достаточно мало, но образовавшийся газ улетучивается, поэтому соль непрерывно диссоциирует для установления равновесия. Последний более устойчив в сухом состоянии ( давление диссоциации 1 мм рт. ст., см. стр. Однако во влажном состоянии он легко разлагается, так как в результате гидролиза превращается в летучие аммиак и двуокись углерода. [10]
Температуру диссоциации СаС03 принято считать равной 898 С. При этой температуре парциальное давление С02 в равновесной системе равно 101 Па. При более низких температурах значительные выходы СаО и С02 достигаются только при достаточном разрежении. Температура в зоне обжига 1100 - 1250 С, так как для полного разложения необходимо прогреть весь кусок известняка для того, чтобы в середине его не оставалось необожженой извести. [11]
Так как температура диссоциации комплекса ниже температуры денатурации ДНК, пришли к заключению, что освобождение РНК ( и ДНК) из комплекса происходит вследствие денатурации белка. Однако вероятно также, что трехцепочечный полинуклеотидный комплекс должен быть менее устойчивым, чем двухцепочечный комплекс. [12]
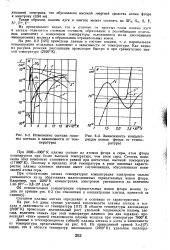 |
Изменение состава плаз.| Зависимость концент. [13] |
В области температуры диссоциации ( 2100 К) происходит значительный рост удельной теплоемкости плазмы элегаза, величина пика при этой температуре намного ( на два порядка) превосходит пик кривой теплоемкости плазмы воздуха при температуре 7000 К. [14]
В отношении температуры диссоциации углекислого магния данные различных исследователей в значительной мере расходятся. [15]
Страницы: 1 2 3 4