Температура - замерзание - водный раствор
Cтраница 2
Молекулярное понижение температуры замерзания водных растворов окиси этилена6 равно dt / N 1 7, где N - число молей окиси этилена, растворенных в 1000 г воды. [16]
Поэтому понижение температуры замерзания водных растворов белка даже при высокой концентрации белка очень мало. [17]
Представляют также интерес температуры замерзания водных растворов этиленгликоля различной концентрации ( табл. 234), поскольку они широко применяются в качестве охлаждающих жидкостей. [18]
В табл. 9 приведены температуры замерзания водных растворов некоторых солей. [19]
Как можно видеть, температура замерзания водных растворов этиленгликоля понижается пропорционально его концентрации ( до 66 объемн. [20]
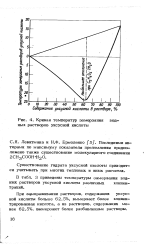 |
Кривая температур замерзания ных растворов уксусной кислоты. [21] |
В табл. 3 приведены температуры замерзания водных растворов уксусной кислоты различных концентраций. [22]
Подобное же ненормально большое понижение температуры замерзания водных растворов, вызванное диссоциацией молекул растворенного вещества, обнаруживает большинство кислот, щелочей и солей. Предположение о распаде ( диссоциации) молекул указанных веществ в водном растворе на частицы более мелкие, чем молекулы, нашло полное подтверждение в теории электролитической диссоциации, разбору которой посвящена следующая глава. [23]
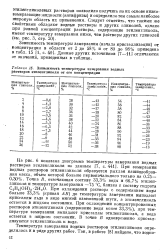 |
Зависимость температуры замерзания водных растворов этиленгликоля от его концентрации. [24] |
На рис. 6 показана диаграмма температуры замерзания водных растворов этиленгликоля по данным [ 7, с. При охлаждении раствора с содержанием воды больше 33 3 % ( кривая АВ) до температуры замерзания выпадают кристаллы льда в виде мягкой взвешенной шуги, а этиленгликоль остается в жидком состоянии. При охлаждении концентрированных растворов этиленгликоля ( содержание воды менее 33 3 %), при температуре замерзания выпадают кристаллы этиленгликоля, а вода остается в жидком состоянии. В точке В одновременно кристаллизуются этиленгликоль и вода. [25]
В табл. 2.2 приведены плотность и температура замерзания водных растворов хлористого кальция различной концентрации. [26]
Важное свойство гликолей - способность понижать температуру замерзания водных растворов, что дает возможность использовать водные растворы гликолей как антигидратный ингибитор при минусовых температурах контакта. [27]
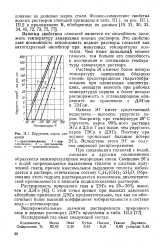 |
Упругость паров гли-па Ров ТЭГа и ДЭГа. Поэтому при колей осушке происходят большие потери. [28] |
Важным сврйством гликолей является их способность понижать температуру замерзания водных растворов. Это свойство дает возможность использовать водные растворы гликолей как антигидратный ингибитор при минусовых температурах контакта. [29]
Исключительно важным свойством гликолей является их способность понижать температуру замерзания водных растворов, в которых они ассоциируют с водой, образуя гидраты. Температура замерзания этих гидратов ниже той, которая теоретически рассчитана для смеси гликоля с водой при концентрации, соответствующей составу гидрата. Характерным свойством гликолей и их растворов является способность к переохлаждению. [30]
Страницы: 1 2 3 4