Температура - затвердевание - расплав
Cтраница 1
Температура затвердевания расплава определяется соотношением между величинами свободных энергий твердой GTB и жидкой Ож фаз. Для того чтобы началась кристаллизация, необходимо некоторое переохлаждение Д7 Однако в действительности при малых переохлаждениях кристаллизация не происходит. При понижении температуры стали увеличивается переохлаждение АГ и поэтому стремление жидкости к самопроизвольному затвердеванию увеличивается. Какова же наименьшая величина AT, при которой может начаться кристаллизация. Оказывается, что кристаллизация любой жидкости происходит не сразу. Сначала в ней образуются микроскопические скопления частиц, в которых уже имеется определенная упорядоченность, характерная для твердого состояния. Эти скопления образуются вследствие случайных отклонений от равномерного распределения, которые всегда имеются в системах с очень большим числом частиц. [1]
 |
Схема установки для измерения скорости кристаллизации. [2] |
С выше температуры затвердевания расплава Го - Часть термостатирую-щей жидкости отводили из термостата в холодильник с температурой / ст t0 и подавали на охлаждение цилиндра. [3]
Обычно пользуются эвтектическими смесями с целью понижения температуры затвердевания расплава. [4]
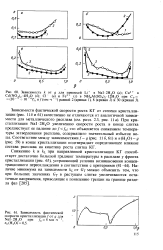
Для примера на рис. 41 построена зависимость температуры затвердевания расплава 10 % LiI03 - 90 % LiN03 от температуры его кристаллизации. Пересечение этой кривой с линией равных температур аЪ дает температуру равновесной кристаллизации нитрата лития в данном расплаве. Положение линии ликвидуса, определяемое методом СТА, совпадает с данными визуально-политермического метода, если начало кристаллизации фиксируется при своевременном введении в расплав затравки кристаллизуемого вещества. [5]
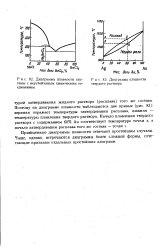 |
Диаграмма плавкости системы с неустойчивым химическим соединением. [6] |
Поэтому на диаграмме плавкости наблюдаются две кривые ( рис. 83): верхняя отражает температуры затвердевания расплава, нижняя - температуры плавления твердого раствора. [7]
 |
Диаграмма плавкости системы с неустойчивым химическим соединением. [8] |
Поэтому на диаграмме плавкости наблюдаются две кривые ( рис. 84): верхняя отражает температуры затвердевания расплава, нижняя - температуры плавления твердого раствора. [9]
Криоскопический метод дает относительно небольшую информацию о термодинамических свойствах растворов расплавленных солей. Этот метод основан на измерении температур затвердевания расплавов солей в зависимости от концентрации компонентов. Криоско пические измерения особенно удобны для определения активности компонентов при температурах, соответствующих кривой ликвидуса. [10]
Криоскопический метод дает относительно небольшую информацию о термодинамических свойствах растворов расплавленных солей. Этот метод основан на измерении температур затвердевания расплавов солей в зависимости от концентрации компонентов. Криоско-пические измерения особенно удобны для определения активности компонентов при температурах, соответствующих кривой ликвидуса. Иногда при изучении расплавленных солей криоскопические измерения дополняют калориметрическими с тем, чтобы получить более полную термодинамическую характеристику системы. Криоскопический метод находит применение в термодинамических исследованиях растворов расплавленных солей в тех случаях, когда другие методы не вполне пригодны. [11]
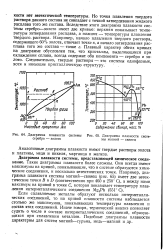 |
Диаграмма плавкости системы [ IMAGE ] Диаграмма плавкости систе-серебро - золото мы магний - свинец. [12] |
Но точка плавления твердого раствора данного состава не совпадает с точкой затвердевания жидкого расплава того же состава. Вследствие этого диаграмма плавкости системы серебро-золото имеет две кривые: верхняя показывает температуры затвердевания расплава, а нижняя - температуры плавления твердого, раствора. Например, начало плавления твердого раствора, содержащего 60 % золота, отвечает точке в, а начало затвердевания расплава того же состава - точке г. Плавный характер обеих кривых на диаграмме обусловлен тем, что кристаллы, выделяющиеся при охлаждении сплава, всегда содержат оба компонента - серебро и золото. Следовательно, твердые растворы - это системы однофазные, хотя и имеющие кристаллическую структуру. [13]
В силу этого только часть введенного кремнезема образует частицы новых видов. Именно этими обстоятельствами, а не обособленными существованием димеров ( SiO2) 2 вызывается меньшее понижение температуры затвердевания расплава. [14]
Страницы: 1 2