Температура - разложение - гидрат
Cтраница 1
Температура разложения гидратов зависит от энергии связи между молекулами гидратообразователя и воды. Ван Аркель и де Бур указали, что молекулы гидратообразователя связываются с молекулами воды следующим образом. Находящиеся во внешней сфере комплекса гидрата дипольные молекулы воды поляризуют находящуюся в центре комплекса молекулу гидратообразователя и вызывают в ней образование индуцированных электрических моментов. Вследствие электрического взаимодействия постоянных диполь-ных моментов молекулы воды и индуцированных моментов в молекуле гидратообразователя происходит образование молекулы гидрата. Однако Лондон [1] указал, что одним электростатическим взаимодействием нельзя объяснить притяжение двух нейтральных частиц. Действительно, некоторые газы и жидкости, не обладающие дипольным моментом, образуют гидраты. Так, благородные газы не обладают дипольным моментом, но образуют гидраты. [1]
В обзорной таблице Штакельберга [13] приведены: температура разложения гидрата 15 4 С при Р атм; температура верхней квадрупольной точки 16 С; теплота образования гидрата 15000 кал / моль. [2]
У Штакельберга [13] АЯ15 0 ккал / моль, температура разложения гидрата равна 15 8 С при / 1 атм. [3]
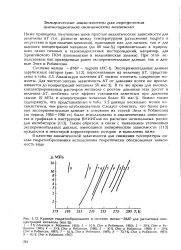 |
Кривые гидратообразования в системе метан - BMP для различных концентраций метанола ( мас. %. [4] |
Ниже приведены полученные нами просгые аналитические зависимосги для величины ДГ ( т.е. разности между температурами разложения гидрата в отсутствие и при наличии метанола), пригодные как для низких, так и для высоких концентраций метанола ( до 80 мас. При этом использованы как приведенные ранее экспериментальные данные, так и данные Энга и Робинсона. [5]
Чтобы выяснить причины этою явления, надо было сравнить приза-бойную температуру газа с равновесной температурой гидратообразова-ния, а также с температурой разложения гидратов в тех же условиях. Для этого была произведена дополнительная обработка результатов испытания скв. [6]
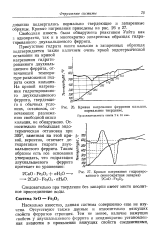 |
Кривая нагревания гидратиро. [7] |
Присутствие гидрата окиси кальция в запаренных образцах подтверждается также наличием очень яркой эндотермической остановки на кривой нагревания гидрати-рованного двухкальциевого феррита, отвечающей температуре разложения гидрата окиси кальция. [8]
Существующие методы перевода газа из гидратного в свободное состояние основываются на снижении пластового давления ниже давления разложения гидрата; на повышении температуры залежи или ее части выше температуры разложения гидрата, а также на свойстве гидратов газов разлагаться при их контакте со спиртами и другими жидкостями. [9]
По номограмме [1] для газа метанового состава, каким является газ Мессояхского газового месторождения, и значениям рс на каждом режиме испытания находились равновесная температура образования Тт и температура разложения Тр гидратов. Учет температуры Т необходим из-за весьма малого периода времени простаивания скважины при переходе от режима к режиму, что обусловливает частичное или полное сохранение гидратов за этот период. [10]
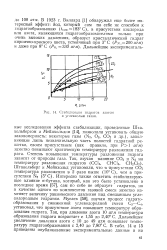 |
Стабилизация гидратов азотом и углекислым газом. [11] |
Шта-кельбергом и Мейнхольдом [14], позволили установить общую закономерность: некоторые газы ( N2, О2, СО2 и др.), заполняющие лишь незначительную часть полостей гидратной решетки, своим присутствием ( как правило, при Р атм заметно повышают критическую температуру разложения гидрата. Степень повышения температуры разложения гидрата зависит от природы газа. Интересно также отметить стабилизирующее влияние м-бутана, который, как это было установлено в последнее время [57], сам по себе не образует гидратов, но в качестве одного - из компонентов газовой смеси заметно изменяет величину равновесного давления над смешанным углеводородным гидратом. Мусаев [58], изучая процесс гидрато-образования у сжиженной углеводородной смеси С3 - С4, установил, что присутствие азота повышает температуру образования гидрата. Так, при давлении азота 10 атм температура образования гидрата возрастает с 1 55 до 2 40 С. Дальнейшее увеличение давления азота с 10 до 49 атм повышает температуру гидратообразования с 2 40 до 7 80 С. [12]
Под атмосферным давлением метановый гидрат разлагается при - 84 43 С, а этановый при - 28 9е С. Для природного газа температура разложения гидрата примерно равна - 74 С под тем же давлением. [13]
Результаты проведенных опытов позволяют сделать следующие выводы: углеводородные растворители могут быть применены в качестве ингибиторов кристаллогидратообразования; введение в природный газ углеводородного растворителя ( пироконденсата) позволяет снизить равновесную температуру кристаллогидратообразования. Эффект достигается за счет повышения температуры разложения гидратов. [14]
При определении воды в гидратах во многих случаях весьма важное значение имеет выбор переносящего агента. Обычно его температура кипения должна быть равной температуре разложения гидрата или более высокой. [15]
Страницы: 1 2