Температура - титруемый раствор
Cтраница 2
После того как в колбы налит раствор оксалата, нужно создать условия, при которых нацело протекает реакция между оксалатом и перманганатом: первым условием является кислая среда, а вторым - температура титруемого раствора около 60 С. [16]
Вблизи конечной точки титрования титрант вводят медленно, по каплям. Температура титруемого раствора должна быть в пределах 20 - 25 С. [17]
Калориметрический или термометрический метод. Измеряя термометром или термопарой изменение температуры титруемого раствора, можно приближенно определить тепловой эффект происходящей при титровании реакции. [18]
Как известно, большинство химических реакций сопровождается выделением или поглощением тепла. При экзотермической реакции титрования по мере подачи титранта температура титруемого раствора повышается и достигает максимальной величины в конечной точке титрования. [19]
Как известно, большинство химических реакций сопровождается выделением или поглощением тепла. При экзотермической реакции титрования по мере подачи титрующего вещества температура титруемого раствора повышается и достигает максимальной величины в конечной точке титрования. [20]
Щелочность выражают числом миллиграмм - или микрограмм-эквивалентов кислоты, расходуемых на 1 л воды. При титровании должны соблюдаться определенные условия в отношении количества вводимого индикатора, а при пользовании метилоранжем также и в отношении температуры титруемого раствора. [21]
Определение кремнефтористого натрия ( NajSiFe) Навеску вещества ( около 1 г) растворяет в колбе Эрленмейера, емкостью в 250 мл, в 100 мл горячей воды, свободной от углекислоты. N раствором щеЗючи до появления розовой окраски; после этого нагревают до кнпе-вия и снова титруют до неисчезающей розовой окраски, поддерживая температуру титруемого раствора близкой к температуре кипения. [22]
Термометрическое титрование кислот и оснований отличается еще меньшей чувствительностью. Известно, что при нейтрализации 1 г-экв сильной кислоты сильным основанием ( или наоборот) выделяется 13700 кал. Для построения кривой титрования и нахождения точки эквивалентности температура титруемого раствора должна повыситься в процессе титрования хотя бы на 0 1 С, конечно, при условии хорошей теплоизоляции и возможности контролировать малые изменения температуры с достаточной точностью. [23]
Вейган и его сотрудники [1, 4, 5] применили катали-метрический метод для определения третичных аминов и солей органических кислот, использовав в качестве титранта хлорную кислоту. Основания растворяли в ледяной уксусной кислоте, содержащей небольшие количества воды ( 2 % объемн. При прибавлении стандартного раствора хлорной кислоты, изменение температуры титруемого раствора, обусловленное реакцией небольшого количества присутствующего основания, идет медленно до эквивалентной точки. После достижения эквивалентной точки в растворе появляется маленький избыток хлорной кислоты. Хлорная кислота катализирует реакцию между водой и уксусным ангидридом. Температура раствора при этом резко поднимается и конечная точка титрования для реакции нейтрализации четко обозначается. При более низких концентрациях оснований повышается ошибка определения. При определении таких оснований, как аденин и цинхонин, и таких солей, как бифталат калия, получены результаты, отличающиеся в среднем меньше чем на 0 3 % от результатов, полученных потенциомет-рическим методом. [24]
Искривление обусловлено неполнотой протекания реакции. Такие кривые обрабатывают методом экстраполяции. Небольшой наклон, участка АВ вызван частичным выравниванием температуры пробы и окружающей среды. Наклон участка CD обусловлен отчасти этой же причиной, а отчасти разностью температур титруемого раствора и титранта. [25]
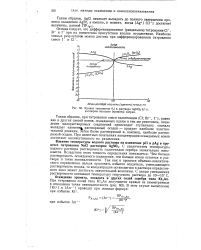 |
Кривая титрования 0 1 н. раствора AgNO3 0 1 н. раствором оксалата ( хромата натрия. [26] |
С увеличением температуры водного раствора растворимость галогенидов серебра значительно повышается. Вследствие этого точность определения понижается. Чем больше растворимость осаждаемого соединения, тем больше ионов остается в растворе в точке эквивалентности. Так как в процессе объемно-аналитического определения нельзя приливать избыток осадителя, уменьшающего растворимость осадка, то концентрация остающегося в растворе определяемого иона может достигать значительной величины. С целью уменьшения растворимости понижают температуру титруемого раствора до ГО-15 С. [27]
С увеличением температуры водного раствора растворимость галогенидов серебра значительно повышается. Вследствие этого точность определения понижается. Чем больше растворимость осаждаемого соединения, тем больше ионов остается в растворе в точке эквивалентности. Так как в процессе объемно-аналитического определения нельзя приливать избыток осадителя, уменьшающего растворимость осадка, то концентрация остающегося в растворе определяемого иона может достигать значительной величины. С целью уменьшения растворимости понижают температуру титруемого раствора до 10 - 15 С. [28]
Большинство химических реакций сопровождается заметным изменением энтальпии системы, которое проявляется в виде наблюдаемого изменения температуры системы. Для термометрического титрования пригодны как экзотермические, так и эндотермические реакции, протекающие в водных и неводных растворах. Измеряют тепловой эффект при титровании. Титрант добавляют непрерывно, происходит изменение температуры по мере введения титранта. Обычно пользуются раствором титранта относительно высокой концентрации, это позволяет пренебречь влиянием разбавления на изменение температуры титруемого раствора. Соблюдают постоянство условий титрования, в частности начальные температуры титруемого раствора и титранта должны быть одинаковыми. [29]
Химическая комиссия ( см. выше) указывает также на следующие обстоятельства, которые необходимо учесть при точной работе. При холостых определениях как малый, так и большой избыток окиси цинка вызывают одинаковый расход марганцовокислого калия, составляющий обычно меньше 0 1 мл; его необходимо учесть при последующем титровании. Сернокислых растворов и сернокислых солей следует избегать, так как в их присутствии расход марганцовокислого калия оказывается слишком малым. Избыток окиси цинка в присутствии азотнокислых солей и хлористых металлов не оказывает существенного влияния на результат титрования. То же относится и к степени разбавления раствора, подлежащего титрованию. Если требуют разбавлять по меньшей мере до 400 мл, то этим только хотят уменьшить охлаждение раствора, вызванное прибавлением марганцовокислого калия, так как опыты показали, что наибольший расход марганцовокислого калия имеет место в кипящих или почти кипящих растворах; во всяком случае температура титруемого раствора не должна быть ниже 80 С. Не безразлично также и то, производится ли прибавление марганцовокислого калия в несколько приемов и постоянно ли взбалтывают во время при-ливания титрованного раствора; в обоих случаях расход оказывается меньше истинного. Если установленное предварительным опытом количество марганцовокислого калия прибавить из бюретки сразу, то расход его оказывается больше, если сильно взболтать жидкость только в конце титрования. Полученные таким образом величины приближаются к теоретической и почти совпадают с результатами, которые получаются, если прибавить избыток марганцовокислого калия и потом титровать его обратно - безразлично чем, мышьяковистой кислотой или раствором соли закиси марганца. [30]
Страницы: 1 2 3