Разная температура
Cтраница 3
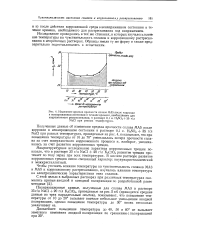 |
Изменение предела прочности сплава МА5 после коррозии. [31] |
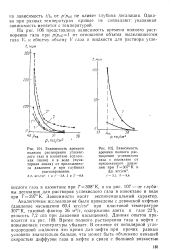
NaCl при разных температурах, приведенные на рис. 4, показывают, что при повышении температуры от 10 до 70 уменьшалась потеря прочности сплава за счет поверхностного коррозионного процесса и, наоборот, увеличивалась за счет развития коррозионных трещин. [32]
Жаропрочность при разных температурах чаще всего оценивается по длительной прочности в виде сводного графика, где каждая линия показывает длительную прочность при определенной температуре ( фиг. [33]
При нескольких разных температурах все эти соотношения оставались практически неизменными. Таким образом, относительные скорости изучаемой реакции определяются каким-то кинетическим фактором, по-видимому, мало зависящим от температуры. Как видим, скорости разрыва связей бив весьма близки; возможно, что выбор направления разрыва определяется здесь преимущественно законом случая. Наоборот, большая или меньшая трудность разрыва связи а, по-видимому, зависит от природы радикала. Дальнейшие исследования должны показать, сколь велико это влияние при более широком выборе разных типов радикалов. [34]
Однако при разных температурах кривые не совпадают: указанная зависимость меняется с температурой. [36]
Винипласт при разных температурах стоек к следующим агрессивным средам: до 80 С - к озону, до 60 С к газообразному аммиаку ( 100 %), газам, содержащим HF ( влажным), содержащим серную кислоту, топочным сухим, едкому кали ( до 60 %); насыщенному бромноватистокислому, азотнокислому, цианистому, марганце-вокислому ( 6 %), хлористому и перхлорату ( 1 %) калия; насыщенному хлористому кальцию и азотнокислому ( до 50 %); разбавленным квасцам, кислороду любой концентрации; кислотам - бромисто-водородной ( 48 %), винной ( насыщенной), гликолевой, кремне-фтористоводородной ( до 32 %), лимонной ( насыщенной), надхлорной ( насыщенной), олеиновой ( продажной), серной ( до 80 %), соляной ( до 37 %), стеариновой, уксусной ( до 60 %), щавелевой ( насыщенной), жирным; насыщенному сернокислому и хлористому магнию; мочевине ( до 33 %); насыщенному, сернистому, хлористому и хлорноватистому натрию, едкому натру ( до 60 %), насыщенному уксуснокислому свинцу, сухому сернистому газу, сухой газообразной углекислоте, формалину ( до 40 %) - насыщенному сернокислому и хлористому цинку. [37]
Основывается на разных температурах кипения компонентов. По условиям проведения различают три вида перегонки: 1) при атмосферном давлении; 2) при пониженном давлении ( перегонка в вакууме); 3) с водяным паром. В зависимости от соотношения между температурами кипения составных частей смеси используют простую или фракционную перегонку. Аппаратурное оборудование перегонки зависит от количества перегоняемого вещества. В лабораторных условиях можно перегнать от нескольких капель до нескольких литров жидкости, в химическом производстве объемы перегонных аппаратов достигают сотен кубических метров. [38]
Константы равновесия для разных температур по формуле ( 12) и ( 13) можно вычислить лишь в том случае, если для изучаемой реакции известна константа равновесия, хотя бы для одной какой-либо температуры. [39]
Мп рассчитаны для разных температур, их значения можно найти в справочнике. [40]
Возьмем два тела разной температуры и приведем их в соприкосновение друг с другом. Опыт показывает, что от тела с более высокой температурой будет передаваться некоторое количество тепла ( энергии) теплопроводностью к телу, которое имеет более низкую температуру. Из определения количества тепла следует, что имеет смысл говорить только о количестве переданного тепла ( энергии) от одной системы к другой, но не имеет смысла говорить, что система содержит такое-то количество теплоты. [41]
Расчет равновесия для разных температур по формулам ( VII, 11) и ( VII, 12) возможен лишь при использовании константы равновесия, известной хотя бы для одной какой-либо температуры. [42]
Определив х для разных температур, можно построить кривую кипения. [43]
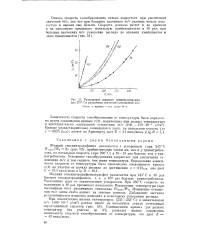 |
Разложение жидкого триннтроанилина при 275 С и различных значениях отношений m / v. [44] |
Совмещением кривых для разных температур ( на участке до 6 % распада) можно определить зависимость скорости газообразования от температуры, что дает Е 43 ккал / молъ. [45]
Страницы: 1 2 3 4