Низкая температура - реакция
Cтраница 1
Низкая температура реакции ( 0 С и ниже) поддерживается обычно введением льда в реакционную массу или охлаждением рассолом через рубашку аппарата. [1]
Низкая температура реакции ( порядка 100 - 150), характерная для жидкофазного окисления, привлекает к этим процессам внимание с точки зрения получения ценных продуктов окисления. [2]
Однако низкой температуре реакции соответствует весьма малая скорость ее, а при применении высокого общего давления должна быть ограничена молярная доля водяного пара в реакционной смеси вследствие того, что при температурах ниже критической температуры воды ( / кр. [3]
При низкой температуре реакции обрыва наблюдаются редко и поэтому получаются длинные реакционные цепи. Таким образом, мы, ириходпм к важному заключению, что между механизмом ступенчатой полимеризации и мехапизмом цепной полимеризации не существует резкого различия, а только некоторая градация. [4]
При низкой температуре реакции обрыва наблюдаются редко и поэтому получаются длинные реакционные цепи. Таким образом, мы приходим к важному заключению, что между механизмом ступенчатой полимеризации и механизмом цепной полимеризации не существует резкого различия, а только некоторая градация. [5]
При низких температурах реакции, свежее сырье вводится в больших количествах, при высоких - его требуется значительно меньше. [6]
При низких температурах реакции образуются вторичные ал-килгидроперекиси, которые распадаются в основном на муравьиный альдегид и первичный спирт. При высоких температурах образуются главным образом вторичные спирты. [7]
При низких температурах реакции ( 20 С) образуются преимущественно орто - и / гора-изомеры, с увеличением температуры реакции увеличивается содержание в смеси мета-изомеров. [8]
При низких температурах реакции протекают настолько медленно, что превращением реагентов можно пренебречь. Теперь предположим, что температура в реакторе повышается. [10]
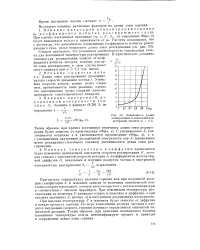 |
Зависимость длины зоны реакции от начальной концентрации топлива ( е 0 1. [11] |
При низких температурах реакции горения или при медленной реакции газификации k в основном зависит от величины кинетической константы скорости реакции k, которая резко возрастает с ростом температуры в соответствии с законом Аррениуса. При повышении температуры реагирования на величину k начинают влиять и кинетика и диффузия, а при высоких значениях Si ( малых е) и внутренняя реакционная поверхность. [12]
В области низких температур реакции протекают медленно и задерживают течение всего процесса. Повышение температуры увеличивает скорость этих реакций и тем самым и всего процесса фотосинтеза в целом. В области температур, близких к оптимальной, скорость темновых реакций приближается к максимальной и повышение температуры сказывается в меньшей степени. [13]
Важное значение имеют поддержание низкой температуры реакции и применение эквивалентных количеств алкена. При высокой температуре или в присутствии избытка алкена протекает реакция диме-ризации, ведущая к загрязнению целевого продукта. [14]
Следовательно, несмотря на низкую температуру реакции, формально происходит одновременно дегидрирование изобутана и алкилирование бензола. Такой процесс дегидроалкилирования удовлетворительно объясняется механизмом реакции с образованием карбониевого иона. [15]
Страницы: 1 2 3 4
