Оптимальная температура - окисление
Cтраница 2
Более удовлетворителыными оказались окислы молибдена, урана и других металлов V и VI групп периодической системы. Лучшие результаты были получены при употреблении смесей таких окислов... Оптимальная температура окисления лежит около 475, а время контакта газов с катализатором - около 0 5 сек. [16]
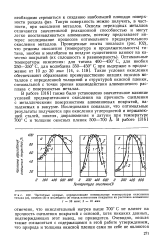 |
Частотные кривые, определяющие оптимальные температуры окисления титана ( а, ниобия ( б и молибдена ( в перед нанесением покрытия из расплава алюминия. [17] |
Окислы переходных металлов отличаются значительной реакционной способностью и могут легко восстанавливаться алюминием, поэтому представляет интерес исследование процессов оптимального предварительного окисления металлов. Оптимальные температуры окисления: для титана 400 - 450 С, для ниобия 250 - 350 С, для молибдена 350 - 450 С при выдержке в продолжение от 10 до 30 мин [ 14, с. Такие условия окисления обеспечивают образование преимущественно низших окислов металлов с определенной толщиной и структурой окисной пленки, оптимальной с точки зрения взаимодействия алюминиевого расплава с поверхностью металла. [18]
Повышение температуры также значительно ускоряет процесс окисления фенолов активным хлором. Однако повышать температуру выше 45 не следует, так как при этом гипохлориты переходят в хлораты, которые обладают меньшей окислительной способностью и замедляют реакцию окисления. Оптимальной температурой окисления является 40 С. При этой температуре скорость реакции увеличивается в 2 - 3 раза по сравнению со скоростью реакции при комнатной температуре. [19]
В одном и том же процессе, в зависимости от условий, оптимальная температура может изменяться на сотни градусов. Так, например, окисление SO2 в SO3 в гомогенной газовой среде заметно происходит лишь при температурах, близких к 1000 С. На окисножелезном катализаторе оптимальная температура окисления находится в пределах 800 - 650 С, на ванадиевом - 600 - 400 С, а на платиновом катализаторе снижается до 350 С при высокой степени окисления. [20]
Образец нагревают почти до белого каления, а улетучивающиеся пары окисляют на нагретой докрасна платине. Этот метод дает достаточно воспроизводимые результаты для различных полиорганосилоксанов. Каждый тип полимера имеет свою оптимальную температуру окисления в трубке для сожжения. Для алифатических групп температура окисления понижается с увеличением длины цепи. Эта методика медленная, но позволяет одновременно определять углерод, водород и кремний. [21]
Для промышленных платиновых катализаторов энергия активации составляет 17 ккал / моль. Поскольку эта величина определялась статическим методом, поправку на изменение времени соприкосновения с температурой вводить не нужно. Кажущаяся молекулярность контактного процесса на платине по двуокиси серы равна единице ( см. стр. Оптимальные температуры окисления двуокиси серы на платиновых катализаторах ( табл. 28), благодаря меньшей энергии активации, приблизительно на 15 ниже соответствующих температур окисления на ванадиевых катализаторах. [22]
Это сокращение зависит от природы сырья, условий и глубины окисления. Улучшается также качество битумов - повышаются пенетрация и растяжимость при 25 С. Оптимальной температурой окисления, как и при обычном окислении остатков смеси татарских нефтей, здесь является 250 С. С повышением температуры окисления до 300 С эффективность хлорного железа снижается. [23]
Это сокращение зависит от природы сырья, условий и глубины окис ления. Улучшается также качество битумов - повышаются пенетрация и растяжимость при 25 С. Оптимальной температурой окисления, как и при обычном окислении остатков смеси татарских нефтей, здесь является 250 С. С повышением температуры окисления до 300 С эффективность хлорного железа снижается. [24]
Для разных процессов оптимальные температуры могут быть ниже нуля или превышать тысячу градусов. В одном и том же процессе в зависимости от условий оптимальная температура может изменяться на сотни градусов. Так, например, окисление SO2 в 5Оз в гомогенной газовой среде заметно происходит лишь при температурах, близких к 1000 С. На окисно-желез-ном катализаторе оптимальная температура окисления находится в пределах 800 - 660 С, на ванадиевом 600 - 400 С, а на платиновом катализаторе снижается до 850 С при высокой степени окисления. [25]
С повышением температуры окисления снижаются расход воздуха и доля кислорода в окисленном битуме. Оптимальной считается температура 250 С. При более высокой температуре в битумах снижается концентрация сложноэфирных групп, увеличиваются скорости реакций дегидрирования, образования кокса и ухудшается показатель хрупкости. При низких температурах ( 230 С) в битумах возрастает содержание слабых кислот. Однако каких-либо закономерностей на все случаи нет, и для каждого вида сырья желательно исследовательским путем определить эффективную оптимальную температуру окисления, при которой получался бы битум заданного качества. [26]
В настоящее время достаточно работ проведено в области окисления гудронов. По мнению Семенова и Эмануэля, при жидкофазном окислении органических соединений по мере увеличения продолжительности процесса окисления идет накопление кислородсодержащих продуктов реакции. Проведенные исследования по распределению кислорода по функциональным группам в битуме тюбеджикской нефти без добавки и с добавкой кислого гудрона / 15 / показали, что с увеличением температуры окисления и расхода воздуха доля функциональных групп уменьшается. Это объясняется ростом соотношения углерода - углеродных связей к сложио ефирным и повышением эффективности передачи кислорода при повышенной температуре. Из вышеизложенного следует, что оптимальной температурой окисления является 250 С при расходе воздуха 5 л / мин. Однако известно, что при температурах ниже 250 С или выше в процессе окисления увеличиваются побочные реакции и потребление кислорода на образование сложно-эфирных групп и также при низких температурах процесса и расхода воздуха, окисление протекает медленно. При температуре окисления 220 С и расходе воздуха 5 л / мин продолжительность окисления увеличивается. Дальнейшее увеличение температуры до 280 С и расход воздуха 5 л / мин уменьшает продолжительность окисления, т.е. на формирование получаемого продукта оказывают влияние термические факторы, а не окислительные. [27]
Страницы: 1 2