Теоретическая температура - сгорание
Cтраница 1
Теоретическая температура сгорания Та принимается равной температуре, которую имели бы газы при адиабатическом сгорании топлива. Она рассчитывается по величине полезного тепловыделения в топке QT, равного теплосодержанию продуктов сгорания топлива при теоретической температуре ta [ C ] и избытке воздуха в конце топки. [1]
Теоретическая температура сгорания Та принимается равной температуре, которая имела бы место при адиабатическом сгорании топлива. Она рассчитывается по величине полезного тепловыделения в топке Qm, которое приравнивается теплосодержанию газов при теоретической температуре ta С и избытке воздуха в конце топки. [2]
Теоретические температуры сгорания различных газов в теоретически необходимом количестве воздуха существенно не отличаются, несмотря на большую разницу в теплотворной способности этих газов. Это объясняется тем, что газы с большей теплотворной способностью требуют соответственно большего количества воздуха для сгорания. [3]
 |
Зависимость степени диссоциации СО2 и HjO от температуры и парциального давления. [4] |
Теоретической температурой сгорания является температура, дв которой нагрелись бы продукты горения, если на их нагрев затрачивалось не все тепло, внесенное в топку, а тепло за вычетом потерь от химической и механической неполноты сгорания, потерь с физическим теплом шлаков и потерь тепла ст диссоциации газов. [5]
 |
Зависимость степени диссоциации СОгН2О от температуры парциального давления. [6] |
Теоретической температурой сгорания является температура, до которой нагрелись бы продукты горения, если на их нагрев затрачивалось не все тепло, внесенное в топку, а тепло за вычетом потерь от химической неполноты сгорания и потерь тепла от диссоциации газов. [7]
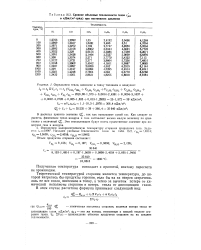 |
Средние объемные теплоемкости газов срт в кДж / ( м - град при постоянном давлении. [8] |
Теоретической температурой сгорания является температура, до которой нагрелись бы-продукты горения, если бы а их нагрев затрачивалось не все тепло, внесенное в топку, а тепло за вычетом потерь от химической неполноты сгорания и потерь тепла от диссоциации газов. [9]
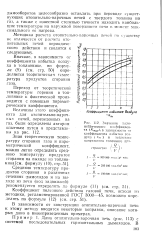 |
Значения пирометрического коэффициента ( Л пи / Л в зависимости от коэффициента избытка воздуха ( я, и теплового напряжения топочного про. [10] |
Зная теоретическую температуру сгорания газа и пирометрический коэффициент, можно легко определить среднюю температуру продуктов сгорания на выходе из топливника [ см. формулу ( 10), стр. [11]
Зная теоретическую температуру сгорания топлива ТТ и температуру продуктов сгорания на выходе из топки Гтоп, переходят к расчету конвективных поверхностей нагрева котельного агрегата. С этой целью вычисляют коэффициент теплопередачи и падение температуры в котельном агрегате из уравнения теплового баланса. [12]
Тл - теоретическая температура сгорания, К, условно принимаемая равной расчетной температуре при адиабатическом сгорании. [13]
Тт - абсолютная теоретическая температура сгорания топлива при заданных условиях, если сжигание производится в рабочем пространстве печи, или температура, с которой газы попадают в рабочее пространство, если сжигание топлива производится в обособленной топке, К; Г м и Гм - абсолютные начальная и конечная температуры материала, К; 7 хг - абсолютная температура газов, отходящих от рабочего пространства печи, К. [14]
Та - абсолютная теоретическая температура сгорания топлива, условно принимаемая равной температуре при адиабатном сгорании; М - расчетный коэффициент, учитывающий влияние относительного местоположения максимума температуры х в топке, определяемый выражением М - А - Вх ( А 0 52; В 0 3); Нл - лучевоспринимающая поверхность нагрева; ат - степень черноты топки; ф - коэффициент сохранения тепла; В - расход топлива; Vc - средняя суммарная теплоемкость продуктов сгорания; П - химический критерий, учитывающий влияние коэффициента избытка воздуха. [15]
Страницы: 1 2 3