Критическая температура - метан
Cтраница 1
Критическая температура метана, как видно из табл. 22, равна - 95 5СС, и, следовательно, метан в недрах может присутствовать только в газовой фазе. Однако частично метан может растворяться в нефти, что, впрочем, едва ли может значительно изменить состав газа. [1]
Критическая температура метана составляет 190 55 К. При более высоких температурах, метан может находиться только в газообразном состоянии вне зависимости от давления. [2]
Поскольку критическая температура метана - 82 1 С, для сжижения его нужно охлаждать ниже этой температуры. [3]
Температура при, молярной доле метана в смеси, равной единице, соответствует критической температуре метана. При молярной доле метана в смеси, равной нулю, точки пересечения линий критических температур с осью ординат соответствуют значениям критических температур углеводородов. [4]
В газоконденсатных месторождениях содержание метана колеблется от 75 до 94 % ( объемных) и так как критическая температура метана составляет - 82 5, то явление обратной конденсации начинается уже от - 53; таким образом, область температур, при которых происходит обратная конденсация, велика по сравнению с областью температур, при которых протекают только нормальные процессы испарения и конденсации. [5]
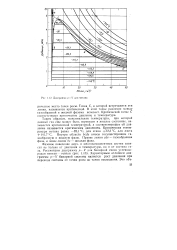 |
Диаграмма /. - V для метана. [6] |
Критическая температура метана равна - 82 1 С, для этана 32 3 С, для азота 141 7 С. [7]
Существующие методики расчета вязкости жидких смесей обладают тем недостатком, что они не позволяют проводить расчеты при температурах, превышающих критические температуры отдельных компонентов. Например, критическая температура метана равна 190 6 К, в то время как в технологических процессах встречаются жидкие смеси и при температурах порядка 400 К, содержащие метан. Для определения поправочных функций, зависящих от температуры, приходится иметь весьма подробные экспериментальные данные в широких интервалах составов. В некоторых методиках необходимо знание плотности смесей. Наконец, использование экспериментальных данных по вязкости отдельных компонентов вблизи линии насыщения, точность которых часто оказывается очень невысокой, снижает и без того сомнительные достоинства этих методик. [8]
Однако применение закона Рауля ограничено, во-первых, тем, что некоторые смеси веществ значительно. Ввиду того, что критическая температура метана составляет 82 С, закон Рауля очень редко можно применить для природных газовых смесей, содержащих метан. [9]
Из табл. 20 видно, что с увеличением интервала выкипания нефтяных фракций их критические температуры растут, а критические давления падают. Критические температуры смесей нефти с метаном значительно ниже, чем у нефтей, так как критическая температура метана равна - 82 5 С. Поэтому критические температуры смесей нефтей с метаном понижаются пропорционально содержанию метана в системе. [10]
Для бинарных смесей метана с углеводородами тяжелее я-декана температура, отвечающая максимальному критическому давлению, не была определена. Следует отметить, что для бинарных смесей метана с углеводородами тяжелее w - пентана критические кривые терпят разрыв в области температур, близких к критической температуре метана. Это связано с тем, что в области разрыва наблюдается трехфазное равновесие типа пар - жидкость - жидкость. [11]
В первом случае применяют весьма низкие температуры - от - 120 до - 160 С. Так, метановая колонна работает при температуре в верхней части от-150 до-158 С ( абсолютное давление 1 5 - 2 am) и в нижней - около - 80 С. Выбор низкого давления и в связи с этим столь глубокого охлаждения объясняется низкой критической температурой метана ( - 82 5 С), а также более высоким значением коэффициента относительной летучести смеси метан-этилен в области низких давлений. [12]
Если охлаждение смеси водорода п легких углеводородов производится при любом постоянном давлении, то путем последовательной конденсации нельзя разделить этилен и метан, несмотря на большую разницу в температурах кипения и, следовательно, в относительных летучестях этих двух углеводородов. При конденсации этилена путем снижения температуры, конденсируются также значительные количества метана, особенно если парциальное давление метана в исходном газе значительно выше парциального давления этилена. Точно также заметные количества этилена остаются в парах до тех пор, пока не произойдет очень сильное снижение температуры. Таким образом, если надо разделить этилен и метан ректификацией, то температура верха деметани-затора должна быть настолько низкой, чтобы в этой части колонны присутствовало бы лишь очень малое количество паров этилена, так как весь этот этилен является безвозвратными потерями. Наивысшая допустимая температура верха деметанизатора - 81 С, критическая температура метана. На практике температура должна быть ниже из-за присутствия в смеси водорода, снижающего парциальное давление метана. [13]
Если охлаждение смеси водорода и легких углеводородов производится при любом постоянном давлении, то путем последовательной конденсации нельзя разделить этилен и метан, несмотря на большую разницу в температурах кипения и, следовательно, в относительных летучестях этих двух углеводородов. При конденсации этилена путем снижения температуры, конденсируются также значительные количества метана, особенно если парциальное давление метана в исходном газе значительно выше парциального давления этилена. Точно также заметные количества этилена остаются в нарах до тех пор, пока не произойдет очень сильное снижение температуры. Таким образом, если надо разделить этилен и метан ректификацией, то температура верха деметанизатора должна быть настолько низкой, чтобы ватой части колонны присутствовало бы лишь очень малое количество паров этилена, так как весь этот этилен является безвозвратными потерями. Наивысшая допустимая температура верха деметанизатора - 81 С, критическая температура метана. На практике температура должна быть ниже из-за присутствия в смеси водорода, снижающего парциа. [14]
На приведенные определения законов Рауля и Дальтона накладываются некоторые ограничения. Очевидно, что давление насыщенного пара любого индивидуального компонента существует только при температурах ниже критической температуры этого компонента. Выше этой температуры для индивидуального компонента не имеется какой-либо точной кривой давления насыщенного пара. Кривые давления насыщенного пара для таких компонентов в условиях более высоких температур могут быть получены путем экстраполяции. Однако способ экстраполяции в большинстве случаев не дает удовлетворительных результатов. Так как критическая температура метана равна - 82 8 С, то очевидно, что для определения констант равновесия, которые могут быть использованы для углеводородных смесей, необходимы некоторые другие методы. [15]
Страницы: 1