Соответствующая критическая температура
Cтраница 3
На рис. 22 приведена диаграмма для системы вода - анилин. Подобные кривые называются кривыми, расслоения. Обе кривые сходятся в точке / С соответствующей критической температуре растворения. Любые точки, лежащие вне кривой АКБ, отвечают гомогенной системе, насыщенным растворам компонентов. Точки, лежащие внутри фигуры АКВА, соответствуют системе, состоящей из двух растворов ( двух слоев), составы которых определяются точками пересечения соответствующей изотермы с кривой АК. [31]
 |
Треугольная фазовая диаграмма ( Т const системы, состоящей из воды и двух солей с общим ионом. [32] |
Жидкие трехкомпонентные системы могут состоять из жидких веществ, как дающих растворы любого состава, так и взаимно ограниченно растворимых. В последнем случае на диаграмме состояния появляется область расслаивания. Фигуративной точке системы, лежащей внутри этой области, отвечают фазовые фигуративные точки двух растворов, на которые распадается система. Так же, как и вдвух-компонентных системах, взаимная растворимость трех компонентов зависит от температуры, и в некоторых случаях при соответствующей критической температуре наступает взаимная неограниченная растворимость всех трех компонентов. Область ограниченной растворимости может иметь различные очертания. [33]
Жидкие трехкомпонентные системы могут состоять из жидких веществ, как дающих растворы любого состава, так и взаимно ограниченно растворимых. В последнем случае на диаграмме состояния появляется область расслаивания. Фигуративной точке системы, лежащей внутри этой области, отвечают фазовые фигуративные точки двух растворов, на которые распадается система. Так же как и в двухкомпонентных системах, взаимная растворимость трех компонентов зависит от температуры, и в некоторых случаях при соответствующей критической температуре наступает взаимная неограниченная растворимость всех трех компонентов. Область ограниченной растворимости может иметь различные очертания. [34]
 |
Диаграмма давление - температура.| Диаграмма давление - объем для метана [ III. 42 ].| Ортобарическая плотность метана [ III. 37 ]. [35] |
Линии, соответствующие постоянной температуре ( такие, как abde на рис. III. Данные изменения плотности насыщенных фаз ( представляющие величины, обратные удельным объемам) приведены на рис. III. Необходимо отметить, что при увеличении температуры удельный объем жидкой фазы увеличивается ( плотность уменьшается), а объем газообразной фазы, наоборот, уменьшается ( плотность растет), причем в критической точке С их удельные объемы и плотности становятся одинаковыми. В точке, соответствующей критической температуре и критическому давлению, становятся одинаковыми и все другие свойства обеих фаз. [36]
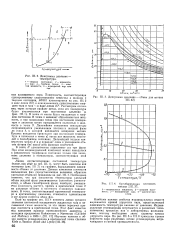 |
Диаграмма температура.| Диаграмма давление - объем для метана ПИ. 42 ].| Ортобарическая плотность метана [ III. 37 ]. [37] |
Линии, соответствующие постоянной температуре ( такие, как abde на рис. III. Данные изменения плотности насыщенных фаз ( представляющие величины, обратные удельным объемам) приведены на рис. III. Необходимо отметить, что при увеличении температуры удельный объем жидкой фазы увеличивается ( плотность уменьшается), а объем газообразной фазы, наоборот, уменьшаемся ( плотность растет), причем в критической точке С их удельные объемы и плотности становятся одинаковыми. В точке, соответствующей критической температуре и критическому давлению, становятся одинаковыми и все другие свойства обеих фаз. [38]
 |
Диаграмма давление - температура.| Диаграмма давление - объем для метана [ III. 42 ].| Ортобарическая плотность метана [ III. 37 ]. [39] |
Линии, соответствующие постоянной температуре ( такие, как abde на рис. III. Данные изменения плотности насыщенных фаз ( представляющие величины, обратные удельным объемам) приведены на рис. III. Необходимо отметить, что при увеличении температуры удельный объем жидкой фазы увеличивается ( плотность уменьшается), а объем газообразной фазы, наоборот, уменьшается ( плотность растет), причем в критической точке С их удельные объемы и плотности становятся одинаковыми. В точке, соответствующей критической температуре и критическому давлению, становятся одинаковыми и все другие свойства обеих фаз. [40]
Иная картина наблюдается при температуре газа Т1 Тк. В этом случае при сближении свободно движущихся молекул на определенное расстояние они попадают в потенциальную яму, глубина которой больше их кинетической энергии. Теперь после соударения молекулы не могут свободно разлетаться в разные стороны. На этом участке вещество существует в двухфазном состоянии: жидкость - газ. Ветвь изотермы слева от точки В соответствует сжатию вещества только в жидком состоянии. На изотерме, соответствующей критической температуре Тк, точки А и В сливаются в одну точку / С, называемую критической точкой. Соответствующие ей давление рк и молярный объем Ук называются критическими. При температурах, выше критической, вещество существует только в газообразном состоянии, и его нельзя перевести в жидкое изотермическим сжатием. [41]
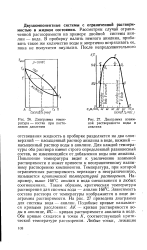 |
Диаграмма взаимной растворимости воды и анилина. [42] |
Для каждой температуры оба раствора имеют строго определенный равновесный состав, не изменяющийся от добавления воды или анилина. Повышение температуры ведет к увеличению взаимной растворимости и может привести к неограниченному взаимному растворению компонентов. Температура, при которой ограниченная растворимость переходит в неограниченную, называется критической температурой растворения. Например, выше 168 С анилин и вода смешиваются в любых соотношениях. Зависимость состава раствора от температуры изображается в виде диаграммы растворимости. На рис. 27 приведена диаграмма для системы вода - анилин. Подобные кривые называются кривыми расслоения: АК. Обе кривые сходятся в точке К, соответствующей критической температуре растворения. [43]
Страницы: 1 2 3