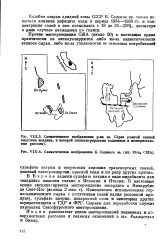
Тенардит
Cтраница 3
В этом методе предполагалось превращение мирабилита в тенардит при летнем испарении рассолов, состав которых попадает в тенардитовое поле системы lNa, Mg2 СГ, SQ2 - - Н20 при 20 - 25 С. Его существенными недостатками являются: зависимость от климатических факторов ( опасность обильных осадков и понижения температуры), плохое использование сырья ( 5 5 т мирабилита на 1 т тенардита), трудности извлечения донного тенардита и его загрязненность другими солями и нерастворимыми примесями. [31]
 |
Диаграмма к задаче № 4. [32] |
Определить извлечение Na2SO4 - из мирабилита в тенардит, если маточный раствор, получаемый при плавлении, охлаждается до 15, а выпавший мирабилит снова подвергается плавлению. [33]
Отсутствие на графике кривизны в изменении Kv тенардита ( эта кривизна характерна для недиффузионных процессов), а также сравнительно высокие значения а и ая позволяют сделать заключение о преобладающем влиянии диффузии в кинетике растворения тенардита. [34]
Возможно осуществлять летнее обезвоживание мирабилита с образованием тенардита в бассейнах под слоем рапы, содержащей NaCl. Этот же процесс протекает и в естественных условиях в некоторых сульфатных озерах. Для выделения тенардита необходимо поддерживать определенный состав испаряемой рапы. Это достигают периодическим добавлением в бассейн с испаряющейся рапой почти насыщенного раствора сульфата натрия, полученного растворением мирабилита в воде. По окончании садки маточный раствор сливают, а тенардит выламывают. Недостатком метода является содержание в нем маточного раствора, для освобождения от которого требуется годовое вылеживание тенардита с периодическим перелопачиванием. Даже и при этом в продукте остается много примесей - NaCl и солей магния. [35]
Природный сульфат натрия встречается в виде минерала тенардита Na2SO4 ( безводный сульфат натрия), мирабилита Na2SO4 - 10Н20, глауберита Na2SO4 CaSO4 и других и залегает в виде твердых отложений или образует рассолы, при выпаривании которых кристаллизуется сульфат натрия. Природный сульфат содержится в огромных количествах в заливе Кара-Богаз - Гол ( Каспийское море), в озере Кучук - ( в Кулундинской степи), в озере Балхаш, в Аральском море, озере Анж-Булат ( Павлодарская область), озере Эбейты ( Омская область) и во многих других районах Советского Союза. Природный сульфат натрия обезвоживают путем плавления ( например, мирабилит) или выпаривания и сушки топочными газами. Обезвоженный сульфат натрия рассыпается в белый порошок. [36]
 |
Kv арканита при. [37] |
Как показывают наши опыты, кинетика растворения тенардита также зависит от диффузионных факторов. [38]
Следовательно, она является безвариантной точкой перехода мирабилита в тенардит в тройной системе. [39]
При 70 состав А распадается на щелок В и влажный тенардит С. [40]
В Европе залежи сульфата натрия в виде мирабилита или тенардита имеются только в Испании и Италии. Комплексное использование горно-химического сырья с получением солей калия ( основной продукт), сульфата натрия, поваренной соли и некоторых других осуществляется в ГДР и ФРГ. Сырьем для переработки служит хартзальц Стассфуртского месторождения. [42]
В штате Аризона находится самое крупное в США месторождение тенардита. Наряду с тенардитом там имеется мирабилит, галит и гипс. [43]
Растворы, фигуративные точки которых лежат в поле кристаллизации тенардита, можно разделить на две группы. При изотермическом испарении этих растворов из них вместе с тенардитом будет кристаллизоваться галит ( вторая соль); затем испарение пойдет по пути, рассмотренному выше на примерах испарения растворов, фигуративные точки которых лежат в поле галита. [44]
Из растворов, точки которых лежат в поле кристаллизации тенардита правее линии ТР2 в качестве второй соли будет выпадать астраханит. При кристаллизации астраханита и тенардита из растворов состава, изображаемых линией P Pz, его фигуративная точка должна удаляться от того и другого полюса. [45]
Страницы: 1 2 3 4