Отведенная теплота
Cтраница 1
Отведенная теплота ft, 3 изображается площадью a. Вся работа I изображается площадью и132Ь, которая на площадь 132 больше, чем / И3) и на площадь 12 3 меньше, чем / ад. Сравнивая рис. 7.12 и 7.13, замечаем, что суммарная работа всасывания и нагнетания при политропном сжатии ( если пК) меньше, чем при адиабатном. [1]
Количество отведенной теплоты равно изменению энтальпии, так как процесс протекает в изобарных условиях. [2]
Аналогично определяется отведенная теплота 02 в процессе 4 - 1: Q2 г / 4 - щ; м418 мм; Uj2 мм; ц4 - 11 мм. [3]
Так как конденсация протекает изохорно, то отведенная теплота равна убыли внутренней энергии. [4]
Так как конденсация протекает изохорно, то отведенная теплота будет равна убыли внутренней энергии. [5]
Таким образом, в рассматриваемом случае количество выделившейся и отведенной теплоты совпало бы с работой, затрачиваемой в компрессоре. [6]
Заметим, что при обратимых процессах подведенная или отведенная теплота в диаграмме s - Т всегда соответствует площади под линией процесса. [7]
Заметим, что при обратимых процессах подведенная или отведенная теплота в диаграмме s - Т всегда соответствует площади под линией процесса. [8]
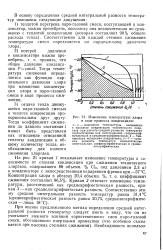 |
Изменение температуры хлора в ходе процесса конденсации. [9] |
Тогда коэффициент сжижения до данного состояния i может быть представлен как отношение отведенной теплоты конденсации к общему количеству тепла, необходимому для полного сжижения хлоргаза. [10]
Отсюда следует, что при изобарных процессах изменение энтальпии равно количеству подведенной или отведенной теплоты. [11]
Изотермический процесс и в этом случае будет предельным, так как при я1 работа, затраченная на сжатие, эквивалентна отведенной теплоте. [12]
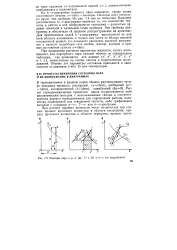 |
Изохоры пара в р - v ( а. Т - s ( б и Л - s ( в координатах. [13] |
Расчет термодинамических процессов паров осуществляется либо аналитическим методом с использованием таблиц и соответствующих формул термодинамики для определения работы, количества подведенной или отведенной теплоты, либо графическим методом с помощью р - v -; Т - s - или / г - s - диаграмм. [14]
Как было отмечено ранее, первый закон термодинамики устанавливает эквивалентность различных форм энергии, соотношение между изменением внутренней энергии, количеством подведенной или отведенной теплоты и совершаемой системой ( или над системой) работой, а также постоянство энергии в изолированной системе. Однако первый закон термодинамики не отражает возможность и вероятность возникновения того или иного термодинамического процесса, связанного с превращением энергии или ее перераспределением. [15]
Страницы: 1 2 3