Интегральная теплота - растворение
Cтраница 2
Интегральные теплоты растворения NaOH для рассчитанных концентраций, которые взяты из справочника, приведены в таблице. [16]
Интегральная теплота растворения полимера может быть измерена калориметрическим методом. Это достигается смешением определенной навески полимера, взвешенного в ампуле, с определенным количеством низком олекулярного компонента, находящегося в калориметрическом сосуде. При соприкосновении с растворителем полимер набухает, а затем растворяется. Процесс в целом, даже при очень малых навесках полимера, продолжается от 20 до 60 мин. Основная трудность при использовании этого метода заключается в том, что в единицу времени выделяется или поглощается очень небольшое количество тепла. Поэтому подобные измерения требуют очень точных приборов и большого умения экспериментатора. Применять большие навески полимеров практически невозможно, так как при этом, во-первых, значительно увеличивается вязкость образующихся растворов, что затрудняет перемешивание, а во-вторых, очень возрастает время тепловой реакции. [17]
Интегральную теплоту растворения определяют экспериментально, а дифференциальную вычисляют по зависимости интегральных теплот растворения от концентрации раствора. [18]
Интегральную теплоту растворения определяют калориметрически. [19]
Интегральную теплоту растворения можно отнести на 1 моль раствора, как это сделано в уравнении ( 1Х 24), или на 1 моль любого компонента. [20]
Интегральную теплоту растворения NaOH ( в кДж / кг), рассчитывают по зависимости, полученной аппроксимацией табличных данных [156] для диапазона изменения концентраций aNaOH 0 1 - 0 425 ( в масс. дол. [21]
Интегральную теплоту растворения относят к 1 моль раствора, поэтому значения г и ДЯт пересчитывают на Xn. [22]
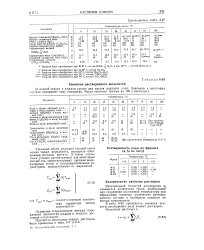 |
Взаимная растворимость жидкостей. [23] |
Интегральной теплотой растворения q / называется количество тепла, необходимое для сохранения постоянной температуры при образовании единицы количества раствора данного состава в изобарном процессе из чистых компонентов. [24]
Интегральной теплотой растворения 1 называется количество тепла, необходимое для сохранения постоянной температуры при образовании единицы количества раствора данного состава в изобарном процессе ив чистых компонентов. [25]
Интегральной теплотой растворения ( ЛЯ, ) называют изменение энтальпии при растворении 1 моль вещества в некотором количестве чистого растворителя. Интегральные теплоты растворения зависят от числа молей растворителя и обычно приводятся в справочнике. Они могут иметь как положительный, так и отрицательный знаки. Знак суммарного теплового эффекта зависит от того, какое из этих слагаемых больше по абсолютному значению. [26]
Интегральной теплотой растворения называют теплоту, поглощенную при растворении одного моля вещества с образованием раствора данной концентрации. В табл. 20 даны интегральные теплоты растворения ряда веществ в воде. [27]
 |
Диаграмма /, с для раствора. [28] |
Интегральной теплотой растворения 7 / называется количество тепла, необходимое для сохранения постоянной температуры при образовании единицы количества раствора данного состава в изобарном процессе из чистых компонентов, имеющих одинаковую температуру. [29]
Полной интегральной теплотой растворения называют изменение энтальпии при растворении одного моля вещества в таком количестве растворителя, которое необходимо для образования насыщенного раствора. Если растворение одного моля вещества происходит в бесконечно большом количестве раствора данной концентрации, тепловой эффект называют дифференциальной или парциальной энтальпией растворения. В этом процессе концентрация раствора остается неизменной, или, точнее, возрастает на бесконечно малую величину, которой пренебрегают. [30]
Страницы: 1 2 3 4