Кинетическое кривое изменение - концентрация
Cтраница 1
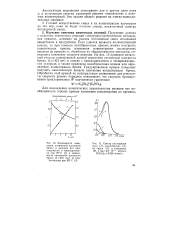
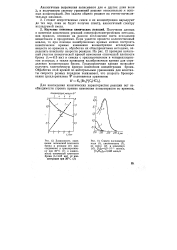
Кинетические кривые изменения концентрации ПЦ в облученных образцах катионита КУ-2 ( Н) после кратковременной ( 10 мин) выдержки их при определенной температуре ( рис. 5.6) свидетельствуют о соизмеримых скоростях рекомбинации ПЦ в набухшем и сухом образцах. В интервале температур 120 - 180 К у обоих образцов наблюдается тенденция к замедлению скорости рекомбинации ПЦ. [2]
Однако характер полученных в настоящей работе кинетических кривых изменения концентрации кислорода в отходящем газе и вычисленных из этих данных Суммарного расходования кислорода и изменения скорости реакции в ходе процесса ( рис. 2) существенно отличается от обычных кривых для такого рода процессов. [3]
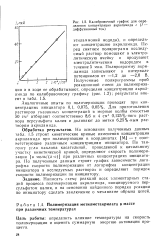 |
Калибровочный график для определения концентрации акриламида с ( I - диффузионный ток. [4] |
На основании полученных данных табл. 1 5 строят кинетические кривые изменения концентрации акриламида при полимеризации в координатах [ MJ - т соответствующие различным концентрациям инициатора. По тангенсу угла наклона касательной, проведенной к начальному участку кинетической кривой, определяют скорость полимеризации [ в моль / ( л-с) ] при различных концентрациях инициатора. По полученным данным строят график зависимости логарифма скорости полимеризации от логарифма концентрации инициатора в исследуемых растворах и определяют порядок скорости полимеризации по инициатору. [5]
Если удается провести количественный анализ, то с помощью калибровочных кривых можно построить кинетические кривые изменения концентрации исследуемых веществ во времени и, обработав их общепринятыми методами, определить константу скорости реакции, Для нахождения кинетических характеристик реакции нет необходимости строить кривью изменения концентрации во времени, а можно использовать зависимость оптической плотности от скорости реакции. [6]
Определение кинетических параметров реакции ( 1) обычными методами представляет большую трудность, так как она протекает очень быстро и практически до конца. Снятие кинетических кривых изменения концентрации исходного продукта аммиака возможно в узких пределах, поскольку дальнейшее повышение содержания МН3 может привести к взрыву аммиачно-воздушных и аммиачно-кислородных смесей. [7]
Получение данных о кинетике химических реакций спект-рофотометрическим методом, как правило, основано на разном поглощении исходными веществами и продуктами. Если удается провести количественный анализ, то обычно с помощью калибровочных кривых можно построить кинетические кривые изменения концентрации исследуемых веществ во времени, и, обработав их общепринятыми методами, определить константу скорости реакции. [8]
 |
Схема экспериментальной установки для исследования кинетики кристаллизации. [9] |
После начала лавинообразного зародышеобразования отбирают 5 - 12 проб раствора в ходе процесса и определяют концентрацию раствора. При достижении конечной температуры кристаллизации прекращается подача воды в рубашку и смесь быстро выливается на фильтровальную бумагу, где кристаллы вещества высушиваются. По полученным значениям концентраций и температур раствора в ходе процесса строятся кинетические кривые изменения концентрации раствора и равновесной концентрации для каждого эксперимента. Так, на рис. 3.18 приведены такие кривые ( где т - время начала кристаллизации), а в табл. 3.3 представлены данные по изменению концентрации и температуры раствора щавелевой кислоты по ходу процесса кристаллизации в одном опыте. [10]
Получение данных о кинетике химических реакций спектрофотометрическим методом, как правило, основано на разном поглощении света исходными веществами и продуктами. Если удается провести количественный анализ, то при помощи калибровочных кривых можно построить кинетические кривые изменения концентрации исследуемых веществ во времени и, обработав их общепринятыми методами, определить константу скорости реакции. На рис. 12 приведен начальный участок кинетической кривой изменения оптической плотности брома ( Я415 км) в смесях с трихлорэтиленом в четыреххлорис-том углероде, а также приведена калибровочная кривая для определения концентрации брома. Градуировочная кривая позволяет получить кинетическую кривую изменения концентрации брома. [12]
Получение данных о кинетике химических реакций спектрофотометрическим методом, как правило, основано на разном поглощении света исходными веществами и продуктами. Если удается провести количественный анализ, то при помощи калибровочных кривых можно построить кинетические кривые изменения концентрации исследуемых веществ во времени и, обработав их общепринятыми методами, определить константу скорости реакции. На рис. 12 приведен начальный участок кинетической кривой изменения оптической плотности брома ( А 415 км) в смесях с трихлорэтиленом в четыреххлорис-том углероде, а также приведена калибровочная кривая для определения концентрации брома. Градуировочная кривая позволяет получить кинетическую кривую изменения концентрации брома. [14]
В подобных случаях проводят определение порядка реакции по начальным скоростям процесса. Практически определение проводят следующим образом. Как и в первом случае, строят кинетическую кртявую по экспериментальным точкам, но фиксируют изменение концентрации реагента на начальном участке, пока скорость реакции приблизительно постоянна. Проводят серию экспериментов с различной начальной концентрацией реагента А. В результате получают несколько ( 4 - 6) кинетических кривых изменения концентрации реагента А. Далее к начальной точке каждой кривой проводят касательную и определяют наклон. Обычно построение касательных не вызывает затруднения, так как начальный участок кинетической кривой слабо искривлен. Если кривизна значительна, то прибегают к помощи зеркала. Прямоугольное зеркало устанавливают так, что отражение кривой в зеркале в заданной точке является плавным без излома продолжением кривой на рисунке. Это означает, что зеркало установлено строго перпендикулярно касательной, которую нужно построить в данной точке. Вдоль нижней грани зеркала проводят прямую, из точки ее пересечения с кривой восстанавливают перпендикуляр. [15]
Страницы: 1