Тетрабутилолово
Cтраница 1
Тетрабутилолово является промежуточным продуктом в циклическом процессе получения дихлорида дибутилолова. Для получения тетрабутилолова по этому методу дихлорид дибутилолова обрабатывают бутилмагнийхлоридом. [1]
Тетрабутилолово не обладает заметной способностью восстанавливать TiCLj, но является хорошим алкилдонором и при взаимодействии с электрофильным А1С1, образует катализатор высокой активности. Вопросы состояния каталитических комплексов и изменения электронной структуры атомов олова в ходе самой полимеризации, по-видимому, могут получить дополнительное освещение благодаря регистрации мессбауэровских спектров. [2]
Затем тетрабутилолово обрабатывают хлорным оловом, чтобы получить дихлорид дибутилолова; применение части этого дихлорида для повторения цикла позволяет получать это соединение с достаточно высоким выходом. Наряду с тетрабутилоловом образуется небольшое количество гексабутилдиолова, которое УТОЖРТ быть превращено в дихлорид дибутилолова расщеплением с помощью хлора до хлористого трибутилолова с последующим взаимодействием с рассчитанным количеством хлорного олова. [3]
 |
Технологическая схема получения диалкилкярйокйшатов олова. [4] |
Органический с: лой отделяют, отгоняют от него бензол и эфир, а тетрабутилолово в кубе 3 отгоняют при пониженном давлении, отбирая - фракцию, кипящую при 165 - 170СС ( при 0 266 кПа), и передают на получение дибутил-оловодихлорида. [5]
Определению металлорганических соединений в сточных водах посвящена работа [315], в которой определялись тетраэтил - и тетрабутилолово на колонке 0 85 м Х4 мы; ТН-дробленое стекло; НФ - апиезон ( 1 %); температура 90 или 165 С; ГН - азот; пламенно-ионизационный детектор. [6]
 |
B. Идентификация органических соединений олова в морских осадках с помощью АЭД ( внизу. Вверху - стандартный раствор соединений олова. 1 - пик растворителя. [7] |
Хроматограмма оловоорганиче-ских соединений, выделенных из морской воды и идентифицированных при помощи АЭД [188]: 1 - диметилпентилолово; 2 - тетрабутилолово; 3 - метил-3 - пентилолово; 4 - трибутилпенти-лолово; 5 - дибутилпентилолово; 6 - бутилпен-тилолово; 7 - тетрапентилолово. [8]
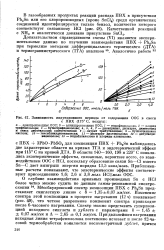 |
Зависимость индукционного периода от содержания ООС в смеси. [9] |
ООС; б - алкглярйпзгодныб GGG; 1 - тетрафеиилилиъи, 2 - хлорид трифснилолова; 3 -бутилтрифенилолово; 4, 5, в, 1 -дикаприлат, дилаурат, диметоксид и окись дибутилолова соответственно; - лаурат трибу тил олова; 9 - бутилстанновая кислота; 10 - гексабутилдистанноксан; 11 - дилаурат диоктилолова; 12 - дибутилди-винялолово; 13 - тетрабутилолово и хлориды алкилолова. [10]
Для повышения светостойкости поливинилхлоридных волокон к смеси стабилизаторов добавляют производные бензофенона. Особенно эффективными ингибиторами оказались органические производные Sn ( например, тетрабутилолово) и РЬ или фосфористые эфиры фенолов. [11]
Хотя один или большее число из рассмотренных механизмов реакции обрыва цепей может быть приписано большинству реакций полимеризации на катализаторах Циглера, различие в микроструктуре полимеров, получаемых при использовании разнообразных каталитических систем, указывает, что различные механизмы реакции, по-видимому, действительно существуют. Например, полиэтилен, полученный в присутствии каталитической системы четыреххлористый титан - тетрабутилолово - хлористый алюминий, содержит 80 - 90 % концевых винильных групп и практически не содержит винилиденовых ответвлений. Такая структура, позволяющая допустить катионный механизм полимеризации, аналогична микроструктуре полиэтилена, синтезированного на катализаторах, состоящих из окислов шестивалентного хрома на носителе, и отличается от структуры полиэтилена, полученного на каталитической системе четыреххлористый титан - триалкилалюминий. [12]
Токсичность в гомологическом ряду резко снижается. Наиболее токсичны тетрам етил - и тетраэтилолово. Тетрабутилолово в 100, а тетрагексилолово в 200 раз менее токсично, чем тетраэтилолово. Соединения с разветвленной цепью более токсичны, чем н-изомеры, триалкильные соединения-более, ди - и моноалкильные - менее токсичны, чем тетраалкильные. Ди-алкнльные вызывают поражение желчных путей и печени, триалкильные - преимущественно центральной нервной системы. Тетраалкильные превращаются в организме в триалкильные. Токсичность триалкильных соединений в значительной степени связана с нарушением проницаемости базальных мембран. Три - и тетраэтилолово подавляют окислительное фосфорилирование, угнетают активность холинэстеразы и 2 4-динитро-фениладенозинтрифосфатазы, вызывают увеличение давления спинномозговой жидкости, проницаемость гематоэнцефалического барьера, судороги, парезы и параличи, пбражение зрительных нервов, отек мозга, нарушение кроветворения. Тетрабутилолово и его производные разрушают миелиновые оболочки в головном мозге и периферических нервах; при хроническом воздействии вызывают гиалиноз стенок сосудов; влияют на кроветворение. [13]
Токсичность в гомологическом ряду резко снижается. Наиболее токсичны тетрам етил - и тетраэтилолово. Тетрабутилолово в 100, а тетрагексилолово в 200 раз менее токсично, чем тетраэтилолово. Соединения с разветвленной цепью более токсичны, чем н-изомеры, триалкильные соединения-более, ди - и моноалкильные - менее токсичны, чем тетраалкильные. Ди-алкнльные вызывают поражение желчных путей и печени, триалкильные - преимущественно центральной нервной системы. Тетраалкильные превращаются в организме в триалкильные. Токсичность триалкильных соединений в значительной степени связана с нарушением проницаемости базальных мембран. Три - и тетраэтилолово подавляют окислительное фосфорилирование, угнетают активность холинэстеразы и 2 4-динитро-фениладенозинтрифосфатазы, вызывают увеличение давления спинномозговой жидкости, проницаемость гематоэнцефалического барьера, судороги, парезы и параличи, пбражение зрительных нервов, отек мозга, нарушение кроветворения. Тетрабутилолово и его производные разрушают миелиновые оболочки в головном мозге и периферических нервах; при хроническом воздействии вызывают гиалиноз стенок сосудов; влияют на кроветворение. [14]
Страницы: 1