Тетрафтороборат
Cтраница 2
Для тетрафтороборатов это соотношение может быть использовано для сравнения устойчивости только немногих из них ввиду отсутствия данных о растворимости большинства тетрафтороборатов. [16]
Анализ тетрафтороборатов представляет собой грудную задачу вследствие сложного равновесия в водных растворах тетрафтороборной кислоты. Более удовлетворительны, по-видимому, гравиметрические методы определения тетрафтороборатов. [17]
Применение тетрафторобората нитрония описано в работах: Olah G. [18]
Кристаллогидрат тетрафторобората никеля отличается от кристаллогидратов тетрафтороборатов Mg, Cd, Sr, Co и др. более низкой упругостью пара и, следовательно, большей термической устойчивостью. [19]
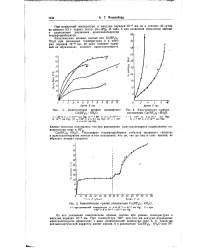 |
Кинетические кривые разложения Co ( BF4 2 6Н2О.| Кинетическая кривая разложения Сц ( ВР4 2 6Н2О. [20] |
Гексагидрат тетрафторобората кобальта проявляет сходстве с кристаллогидратом никеля в том отношении, что он, так же как и соль никеля, не образует низших гидратов. [21]
Растворы тетрафторобората меди в толуоле133 и эфире136 приготовлены при действии металлической меди на растворы тетрафторобората серебра. При выпаривании или при действии влаги происходит диспропорционированяе. [22]
Растворы тетрафторобората меди в толуоле153 и эфире136 приготовлены при действии металлической меди на растворы тетрафторобората серебра. При выпаривании или при действии влаги происходит днспропорционирование. [23]
Из хорошо растворимых тетрафтороборатов наиболее просто получается NH4BF4, так как его растворимость при понижении температуры настолько падает, что он может быть выделен из маточника охлаждением. Для получения соли следует ввести в 40 - 50 % - ную HF теоретическое количество борной кислоты и нейтрализовать полученную тетрафторсборную кислоту аммиаком или углекислым аммонием. Соль может быть очищена как перекристаллизацией, так и сублимацией. [24]
 |
Строение молекул некоторых веществ, в которых все валентные электроны образуют связывающие пары. [25] |
В тетрафтороборате ( Ш) аммония как катион NHJ, так и анион [ BF4 ] - изоэлектронны молекуле метана, и можно предположить, что они имеют сходное строение. Действительно, единственное различие между центральными атомами в частицах NHj, СН4 и [ BF4 ] - состоит в числе протонов в ядрах. [26]
Особо сходны тетрафторобораты, фторсульфонаты и перхлораты, так как радиусы их анионов очень близки. Характерны высокая растворимость литиевых и натриевых солей и солей аквокомп-лексов двухвалентных металлов. Соли калия, рубидия и цезия растворимы относительно мало. Соли с анионом PO Fo мало исследованы, но, првиди-мому, растворимы значительно лучше аналогичных солей других анионов этого ряда. Все же нитроновая соль дифторофосфорной кислоты относительно трудно растворима. [27]
При действии тетрафторобората З - этокси-1 2-дифенилциклопропенильного карбкатиона вместо 3 3-дихлор - 1 2-дифенилцикло-пропена. Обработка Na [ Cr ( CO) 5 ] вместо Ыа2 [ Сг2 ( СО) ш ] приводит к существенно меньшим выходам. [28]
Энтальпия диссоциации твердого тетрафторобората должна отличаться от приведенных выше величин ДЯДИСС. [29]
 |
Данные для определения давления диссоциации некоторых тетрафтороборатов. [30] |
Страницы: 1 2 3 4