Измерение - электродный потенциал
Cтраница 3
Для измерения электродных потенциалов используют разнообразные потенциалметрические установки обычного типа, электронные ( катодные или ламповые) вольтметры и электростатические приборы. [31]
Для измерения электродного потенциала собирают электрическую цепь, состоящую из исследуемого электрода и электрода, потенциал которого известен ( его называют электродом сравнения или полуэлементом), причем электролиты, в которые погружены оба электрода, должны сообщаться друг с другом, а сами электроды должны быть разомкнуты. [32]
Для измерения электродных потенциалов свинцового аккумулятора в качестве вспомогательного электрода применяют кадмиевый электрод, потенциал которого в серной кислоте равен - 0 40 в по отношению к нормальному водородному электроду. [33]
Для измерения электродных потенциалов свинцового аккумулятора в качестве вспомогательного электрода применяют кадмиевый электрод, потенциал которого в серной кислоте равен - 0 4 б по отношению к нормальному водородному электроду. [34]
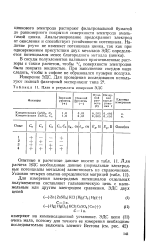 |
План и результаты измерения ЭДС. [35] |
Для измерения электродных потенциалов отдельных полуэлементов составляют гальваническую цепь с каломельным или другим электродом сравнения. [36]
Метод измерения электродных потенциалов полезен для экспрессной оценки способности металлов восстанавливать пассивное состояние, например после механического воздействия на поверхность. Этим метрдом пользуются также при определении склонности сталей к межкристаллитной коррозии, при определении эффективности действия ингибиторов. [37]
Дня измерения электродного потенциала используют компенсационную измерительную схему с нуль-гальванометром. Источником постоянного тока служит сухой элемент. Поскольку ЭДС сухой батареи несколько изменяется во времени, в схему дополнительно включен нормальный гальванический элемент Вестона. Для усиления электродного тока в схему включен ламповый усилитель. [38]
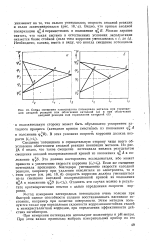 |
Схема смещения электродного потенциала металла при торможении анодной реакции или облегчении катодной ( а и при облегчении анодной реакции или торможении катодной ( б. [39] |
Метод измерения электродных потенциалов очень полезен при быстрой оценке способности сплавов восстанавливать пассивное состояние, например при зачистке поверхности. Этим методом пользуются также при определении склонности коррозионностоиких сталей к межкристаллитной коррозии, при определении эффективности действия ингибиторов. [40]
Схема измерений электродного потенциала металлов компенсированным способом с капиллярным электрометром 2 приведена на фиг. [41]
Схема измерений электродного потенциала металлов приведена на фиг. Измеряемый элемент составляется из стандартного кало-мелевого электрода и электрода исследуемого металла в определенном растворе. [42]
При измерении электродных потенциалов потенциал жидкостной цепи может затруднять определение, создавая добавочную электродвижущую силу. [43]
При измерении электродных потенциалов за нуль принят потенциал нормального водородного электрода. [44]
При измерении электродных потенциалов, как было указано выше, образуют цепь из стандартного водородного электрода ( полуэлемента) и электрода, потенциал которого нужно измерить. Однако практически водородный электрод неудобен в работе. Надо иметь источник водорода, тщательно очищать водород, поступающий в полуэлемент, поддерживать постоянным его давление. Все это создает экспериментальные трудности. Поэтому вместо водородного электрода используют другие, более удобные электроды с постоянным значением потенциала. Наиболее широко применяют каломельный и хлор-серебряный электроды. [45]
Страницы: 1 2 3 4