Pd-электрод
Cтраница 1
Pd-электрод скорость электровосстановления комплексов PdCJj - и PdBr42 - [ 385 1 при одном и том же потенциале возрастает на несколько порядков. Это установлено при потенциалах, расположенных значительно положительнее точки нулевого заряда как ртути, так и палладия, в области высоких объемных концентраций галоген-ионов, при которых степень заполнения ими поверхности обоих электродов, по-видимому, близка к предельной. [1]
Изучена ионизация водорода на полупогруженном Pd-электроде. [2]
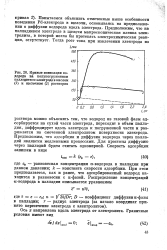 |
Кривые ионизации водорода на полупогруженном палладиевом электроде в кислом 250 ( I и щелочном ( 2 растворах. [3] |
Попытаемся объяснить отмеченные выше особенности поведения Pd-электрода в щелочи, основываясь на предположении о диффузии водорода вдоль электрода. Предположим, что на палладиевом электроде в щелрчи макроскопическая пленка электролита, в которой могла бы протекать электрохимическая реакция, отсутствует. [4]
В качестве примера на рис. 2 приведены изменения потенциалов Pt - и Pd-электродов в отдельности во время титрования Fe раствором бихромата. [6]
Применение этих формул к описанным выше экспериментам в расплавленных карбонатах затруднительно, так как неизвестны значения основных параметров. Pd-электродом в 1 N H2S04 [48] были измерены / - / - кривые при т ] 0 - 510 мв. Скорости электрохимической реакции и адсорбции в кислых растворах очень велики, так что естественно принять предположение о замедленности диффузионной стадии. Однако расчет по формуле (8.45) для диффузионного режима приводит к току J - 200л ( каиа весь периметр электрода, тогда как на опыте получается / - 600 мка. [7]
 |
Зависимость J / J от г 0. [8] |
Применение этих формул к описанным выше экспериментам в расплавленных карбонатах затруднительно, так как неизвестны значения основных параметров. В опытах с полупогруженным Pd-электродом в 1 N H2S04 [48] были измерены J - Z-кри-вые при т ] 0 510 мв. Скорости электрохимической реакции и адсорбции в кислых растворах очень велики, так что естественно принять предположение о замедленности диффузионной стадии. Однако расчет по формуле (8.45) для диффузионного режима приводит к току / - 200 мка на весь периметр электрода, тогда как на опыте получается / - 600 мка. [9]
Эти значения характерны для Pd-электрода. [10]
По активности в реакции электроокисления муравьиной кислоты изученные электроды можно расположить в ряд: Pd Pt - f - 4 Ru Pd - f - Ru Ru; в реакции электроокисления формиат-иона - в ряд: Pd - f - Ru Pd Pt RU Ru. Низкие перенапряжения электроокисления НСООН и НСОО - на Pd-электроде и НСОО - на Pd / Ru-электроде, а также наличие лишь незначительных количеств хемосорбированных продуктов при протекании процесса в стационарных условиях позволили сделать предположение, что в этих случаях процесс электроокисления протекает по механизму дегидрирования. Прочно хемосорбированное вещество выступает при этом в качестве неактивного побочного продукта. Филштих [67] предложил использовать сплавы платины и палладия для окисления метанола, так как присутствие в катализаторе палладия позволяет окислять образующийся в качестве промежуточного продукта НСОО с большой скоростью. [11]
Как установил Хоар, только на Rh, после обработки его в НМОз, так же как и на Pt, удается реализовать обратимый кислородный электрод. Анодные пленки, образованные на Ir, Ru, Os и Pd, позволяют использовать эти электроды в качестве металлооксидных, так как скорость электродных процессов в этих случаях значительно выше, чем для Pt и Аи. Для Pd-электродов характерны самые высокие плотности тока обмена в системе Н / Нг и очень большая растворимость водорода в Pd. [12]
Страницы: 1
