Триоксифлуороны
Cтраница 1
Триоксифлуороны выпадают в осадок при - 20 С в течение длительного времени вследствие постепенного окисления их лейкосоединений кислородом воздуха. [1]
Триоксифлуороны исследованы в основном как реагенты на редкие элементы - сурьму [28], германий [29], титан [30], молибден [31, 32], скандий, цирконий и другие элементы. В литературе появляется все больше работ по аналитическому применению триоксифлуоронов. [2]
Триоксифлуороны исследованы в основном как реагенты на редкие элементы - сурьму I28 ], германий [29], титан [30], молибден [31, 32], скандий, цирконий и другие элементы. В литературе появляется все больше работ по аналитическому применению триоксифлуоронов. [3]
Установлено, что все триоксифлуороны могут служить фотометрическими реактивами для галлия. Лучшими из них являютсятрихлорметилфлу-орон и салицилфлуорон. Молярные коэффициенты погашения комплексов галлия с этими реактивами равны соответственно 6 5 - 10 при 530 ммк и 4 4 - 10 при 540 ммк. [4]
Установлено, что все триоксифлуороны могут служить фотометрическими реактивами для галлия. Лучшими из них являютсятрихлорметилфлу-орон и салицилфлуорон. Молярные коэффициенты погашения комплексов галлия с этими реактивами равны соответственно 6 5 - 10 при 530 ммк и 4 4 - 104 при 540 ммк. [5]
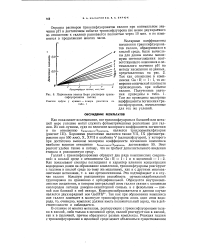 |
Подчинение закону Бера растворов триоксифлуоронатов галлия. [6] |
Как показывает исследование, все триоксифлуороны в большей или меньшей мере успешно могут служить фотометрическими реагентами для галлия. [7]
ФЕНИЛФЛУОРОН ( 2 6 7-триокси - 9-фенил - ЗН-ксантен-3-он; ф-лу см. в ст. Триоксифлуороны), красно-оранжевые крист. [8]
ФЕНИЛ ФЛУОРОН ( 2 6 7-триокси - 9-фенил - ЗН-ксантен-3-он; ф-лу см. в ст. Триоксифлуороны), красно-оранжевые крист. [9]
САЛИЦИЛФЛУОРОН [ 2 6 7-гриокси - 9 - ( 2-оксифенил) - ЗН-ксантен-3-он; ф-лу см. в ст. Триоксифлуороны ], красные крист. [10]
Полуэктовым было установлено, что оксиантрахиноны 1164 ] и другие органические соединения с периоксихинонной группировкой, содержащие хромофор, как краситель, хромотроп 2 В и монооксинафтаценхинонсульфо-кислота 1165 ], в концентрированной серной кислоте реагируют с герма нием, подобно бору. По чувствительности эти реактивы значительно уступают триоксифлуоронам, гематеину и оксифла-вонам. Более чувствительно реагирует с германием ацетилированный хина-лизарин, так называемый ацетилхинализарин. Закону Бера следуют окрашенные растворы с концентрацией германия 0 3 - 3 мкг / мл. [11]
Новые фотометрические реагенты синтезируют и испытывают в настоящее время в ряде аналитических центров. В ГЕОХИ АН СССР на первом месте азосоединения, в одесских лабораториях Института общей и неорганической химии АН УССР ( ИОНХ АН УССР) - триоксифлуороны, в Саратовском педагогическом институте - фталексоны, в Московском университете - различные се-русодержащие соединения. [12]
Страницы: 1