Ионный триплет
Cтраница 1
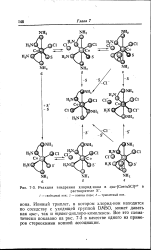 |
Реакция внедрения хлорид-иона в цис - [ Соеп25С1 ] 2 1 в. [1] |
Ионный триплет, в котором хлорид-ион находится по соседству с уходящей группой DMSO, может давать как цис -, так и транс-дихлоро-комплексы. Все это схематически показано на рис. 7 - 3 в качестве одного из примеров стереохимии ионной ассоциации. [2]
К ионным триплетам возможно присоединение еще одного иона. [3]
 |
Кривые проводимости и ионизации применительно к азотнокислому тетраизоамиламмонию в системе дио-ксан - вода. [4] |
Как ни соблазнительна описанная выше теория ионных триплетов, все же не следует делать из нее вывода о безусловной не обходимоети образования детергентами такого рода ионов в углеводородных растворителях. Прежде всего необходимо отметить, что, согласно данным Мэтьюса и Гиршгорна, для объяснения возрастания проводимости такая гипотеза отнюдь не требуется. Данные этих исследователей не являются непосредственно сравнимыми с результатами работы Крауса и Фуосса. Следует предполагать, что поведение коллоида в додекане будет совершенно иным, чем в диоксане. [5]
Интервал изменения величины диэлектрической проницаемости несколько ограничен благодаря тому, что в средах с низкой диэлектрической проницаемостью начинает сказываться образование ионных пар; существенным может оказаться также наличие ионных триплетов и квадруплетов. [6]
 |
Экспериментальные и расчетные значения положения и интенсивности линий люминесцентного спектра GaP. [7] |
В ассоциации могут участвовать больше двух дефектов, и часто такую систему изучать очень трудно. К числу подобных ассоциаций относится ионный триплет, который представляет собой простейшее усложнение рассмотренных выше ионных пар. Если один из дефектов дважды ионизован, как, например, акцептор Zn в Ge, триплет образуется при захвате двух однозарядных доноров. Экспериментально установлено, что образуются также комплексы Li Li Zn2 -, которые могут в некоторой степени снижать диффузионную подвижность. [8]
Метод, предложенный Фуоссом и Краусом, дает возможность рассчитать концентрации ионных триплетов и квадруплетов. [9]
Инертные растворители имеют низкую диэлектрическую постоянную. Растворимость большинства солей в них весьма ограничена, так же как и диссоциация их на ионы. Кроме ионных пар, в этих растворителях легко образуются ионные триплеты и квадруплеты. Карбоновые и другие кислоты димеризуются и полимеризуются с помощью межмолекулярных водородных связей. [10]
О возможном существовании ионных агрегатов, более сложных, чем ионные пары, известно давно. Здесь интересно отметить тот необычный факт, что в определенных условиях заряд катиона может сверх-компенсироваться. Так, в растворе ацетона при 25 С транс - [ Со en 2 NO2H2O ] 24 может присоединить максимум три бромид-иона. Анализы позволяют оценить различные константы скорости взаимного обмена, однако полученная картина довольно сложна, и многие вопросы остаются еще нерешенными. В связи со сказанным выше особенно интересна реакция ыс - [ Соепа DMSOC1 ] 2 ( DMSO - диметил-сульфоксид) с хлорид-ионом в диметилформамиде - типичная и наиболее детально изученная система. На ее примере можно показать, что в условиях, когда реакция не происходит, увеличение концентрации хлорид-иона в растворе приводит к тому, что комплекс существует как в виде свободного иона, так и в виде ионной пары. При дальнейшем повышении концентрации хлорид-иона устанавливается равновесие между ионной парой и ионным триплетом. Скорость образования дихлоро-комплекса возрастает с увеличением концентрации хлорид-иона по мере накопления вещества в виде ионной пары. Последующее увеличение концентрации приводит лишь к росту концентрации ионного триплета за счет ионной пары, но не оказывает значительного влияния на скорость реакции. При этом, однако, меняется основной продукт реакции; если концентрация хлорид-иона низкая, это тра с-дих-лоро-комплекс, если высокая - это ыс-дихлороизомер. Объясняют эти факты следующим образом. Анация ионной пары и ионного триплета происходит с приблизительно равной скоростью, так как в обоих случаях хлорид-ион выходит в координационную сферу после того, как связь кобальта с DMSO диссоциирует. [11]
Как уже было упомянуто, в растворителях с низкой диэлектрической постоянной сила притяжения между ионами, имеющими заряды неодинаковых знаков, довольно значительна по сравнению с растворителями, у которых диэлектрическая постоянная высока. Отсюда следует, что ассоциация неодинаковых ионов, приводящая к образованию нейтральных молекул, намного более вероятна в углеводородных растворителях, чем в воде. Такого рода молекулы являются слабыми проводниками. По мнению Крауса и Фуосса, первоначально наблюдаемое быстрое уменьшение проводимости при низкой концентрации объясняется спариванием указанных ионов. Кривые, иллюстрирующие эту стадию, соответствуют уравнению вида: А С а постоянной величине. Затем кривые проходят через точку минимума, после чего они показывают постепенное возрастание проводимости при концентрации, превышающей указанную точку. Фуосс и Краус предполагают, что за этой точкой находится зона, в которой начинают образовываться ионные триплеты высокой проводимости. [12]
О возможном существовании ионных агрегатов, более сложных, чем ионные пары, известно давно. Здесь интересно отметить тот необычный факт, что в определенных условиях заряд катиона может сверх-компенсироваться. Так, в растворе ацетона при 25 С транс - [ Со en 2 NO2H2O ] 24 может присоединить максимум три бромид-иона. Анализы позволяют оценить различные константы скорости взаимного обмена, однако полученная картина довольно сложна, и многие вопросы остаются еще нерешенными. В связи со сказанным выше особенно интересна реакция ыс - [ Соепа DMSOC1 ] 2 ( DMSO - диметил-сульфоксид) с хлорид-ионом в диметилформамиде - типичная и наиболее детально изученная система. На ее примере можно показать, что в условиях, когда реакция не происходит, увеличение концентрации хлорид-иона в растворе приводит к тому, что комплекс существует как в виде свободного иона, так и в виде ионной пары. При дальнейшем повышении концентрации хлорид-иона устанавливается равновесие между ионной парой и ионным триплетом. Скорость образования дихлоро-комплекса возрастает с увеличением концентрации хлорид-иона по мере накопления вещества в виде ионной пары. Последующее увеличение концентрации приводит лишь к росту концентрации ионного триплета за счет ионной пары, но не оказывает значительного влияния на скорость реакции. При этом, однако, меняется основной продукт реакции; если концентрация хлорид-иона низкая, это тра с-дих-лоро-комплекс, если высокая - это ыс-дихлороизомер. Объясняют эти факты следующим образом. Анация ионной пары и ионного триплета происходит с приблизительно равной скоростью, так как в обоих случаях хлорид-ион выходит в координационную сферу после того, как связь кобальта с DMSO диссоциирует. [13]
О возможном существовании ионных агрегатов, более сложных, чем ионные пары, известно давно. Здесь интересно отметить тот необычный факт, что в определенных условиях заряд катиона может сверх-компенсироваться. Так, в растворе ацетона при 25 С транс - [ Со en 2 NO2H2O ] 24 может присоединить максимум три бромид-иона. Анализы позволяют оценить различные константы скорости взаимного обмена, однако полученная картина довольно сложна, и многие вопросы остаются еще нерешенными. В связи со сказанным выше особенно интересна реакция ыс - [ Соепа DMSOC1 ] 2 ( DMSO - диметил-сульфоксид) с хлорид-ионом в диметилформамиде - типичная и наиболее детально изученная система. На ее примере можно показать, что в условиях, когда реакция не происходит, увеличение концентрации хлорид-иона в растворе приводит к тому, что комплекс существует как в виде свободного иона, так и в виде ионной пары. При дальнейшем повышении концентрации хлорид-иона устанавливается равновесие между ионной парой и ионным триплетом. Скорость образования дихлоро-комплекса возрастает с увеличением концентрации хлорид-иона по мере накопления вещества в виде ионной пары. Последующее увеличение концентрации приводит лишь к росту концентрации ионного триплета за счет ионной пары, но не оказывает значительного влияния на скорость реакции. При этом, однако, меняется основной продукт реакции; если концентрация хлорид-иона низкая, это тра с-дих-лоро-комплекс, если высокая - это ыс-дихлороизомер. Объясняют эти факты следующим образом. Анация ионной пары и ионного триплета происходит с приблизительно равной скоростью, так как в обоих случаях хлорид-ион выходит в координационную сферу после того, как связь кобальта с DMSO диссоциирует. [14]
Страницы: 1