Тензиметрическое измерение
Cтраница 1
Тензиметрические измерения [1-4] при давлении 1 am указывают на неограниченную взаимную растворимость Nb и NbH. Экспериментальные данные разных авторов хорошо согласуются; в работе [3] они получены вплоть до температуры 1400 С, в [1, 2, 4] - только до 700 - 800 С. Определения с помощью вакуумных микровесов [5] соответствуют тензиметрическим измерениям. При температуре 673 С [6] построена кривая давление-состав вплоть до 1000 am, при этом растворимость достигла 42 3 % ( ат. Как видно из изобар ( рис. 244), эквиатомный состав не достигается методами гидрирования. Термодинамические расчеты [4] указывают, что содержание Н не может превысить 47 1 % ( ат. [1]
Выделение двуокиси углерода из таких карбо-натсодержащих силикатных стекол определяется путем тензиметрических измерений в зависимости от температуры. [2]
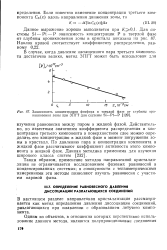 |
Зависимость концентрации фосфора в твердой фазе от глубины проникновения зоны при ЗПГТ для системы Si-Pt - Р. [3] |
Таким образом, применение методов направленной кристаллизации не ограничивается исследованием фазовых равновесий в конденсированных системах; в совокупности с тензиметрическими измерениями эти методы позволяют изучать равновесия с участием паровой фазы. [4]
Из реактора при комнатной температуре он перегонялся в течение нескольких часов под высоким вакуумом в сосуд, охлаждаемый до - 75 С. Так как RhF6 восстанавливается в манометре и реакционном сосуде так быстро, что тензиметрические измерения ненадежны, стехиометрию реакции с ксеноном определяли из веса образовавшегося аддукта с учетом тензиметрически измеренного количества ксенона. [5]
Проводя прецизионные измерения, при которых температуру большого количества вещества, находящегося в стеклянной трубке с эвакуированной рубашкой, определяют термометром сопротивления с точностью до 0ОООГ, можно показать присутствие примесей в количествах до 0 01 мол. Таким образом, по температуре плавления можно установить степень чисто-т ы [29, 30] с определенными ограничениями, подобными тем, которые существуют при тензиметрических измерениях; в последнем случае, несмотря на то что можно установить минимальные примеси легколетучих веществ, малолетучие вещества фиксируются с трудом. [6]
Тензиметрические измерения [1-4] при давлении 1 am указывают на неограниченную взаимную растворимость Nb и NbH. Экспериментальные данные разных авторов хорошо согласуются; в работе [3] они получены вплоть до температуры 1400 С, в [1, 2, 4] - только до 700 - 800 С. Определения с помощью вакуумных микровесов [5] соответствуют тензиметрическим измерениям. При температуре 673 С [6] построена кривая давление-состав вплоть до 1000 am, при этом растворимость достигла 42 3 % ( ат. Как видно из изобар ( рис. 244), эквиатомный состав не достигается методами гидрирования. Термодинамические расчеты [4] указывают, что содержание Н не может превысить 47 1 % ( ат. [7]
Вместо острого пара в колонну регенерации для снижения температуры в некоторых случаях предлагается подавать инертный газ. Возможно также использование углеводородного рецикла в колонне регенерации растворителя. Термическая стабильность ряда полярных растворителей была исследована методом тензиметрических измерений температурной зависимости давления насыщенного пара. [8]
При разбавлении водой это равновесие, естественно, сдвигается влево. Установлено, что при концентрации около 94 мол. Последний, по-видимому, существует в растворах, содержащих 84 мол. Тензиметрические измерения показывают, что при концентрациях кислоты выше 61 4 мол. [9]
При разбавлении водой это равновесие, естественно, сдвигается влево. Установлено, что при концентрации около 94 мол. Последний, по-видимому, существует в растворах, содержащих 84 мол. Тензиметрические измерения показывают, что при концентрациях кислоты выше 61.4 мол. [10]
При разбавлении водой это равновесие, естественно, сдвигается влево. Установлено, что при концентрации около 94 % ( моль. Последний по-видимому, существует в растворах, содержащих 84 % ( мол. Тензиметрические измерения показывают, что при концентрациях кислоты выше 61 4 % ( мол. [11]
Страницы: 1