Изобара - растворимость
Cтраница 2
 |
Система Si02 - НаО, изотермические кривые растворимости кварца ( по Кеннеди. [16] |
На рис. 378 изображена система Si02 - Н20 в виде изобар растворимости кварца в воде по экспериментальным данным Кеннеди. Около каждой кривой указано давление в барах. [17]
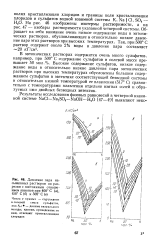 |
Давление пара насыщенных растворов по разрезам с постоянным отношением анионов при 400 С ( а, 150 С ( б и 500 С ( в. [18] |
На рис. 46 изображены изотермы растворимости, а на рис. 47 - изобары растворимости указанной четверной системы. [19]
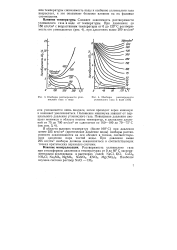 |
Изобары растворимости углекислого газа в воде.| Изобары растворимости углекислого газа в воде. [20] |
В области высоких температур ( более 100 С) при давлении менее 225 кгс / см2 ( критическое давление воды) изобары растворимости заканчиваются на оси абсцисс в точках, соответствующих давлению пара чистой воды. При давлении выше 225 кгс / см2 изобары должны заканчиваться в соответствующих точках критических переходов системы. [21]
Например, в системе K2SO4 - H2O при давлениях 250 и 500 кГ / см - ( PQ 670 кГ / см2) изобары растворимости направляются влево ( отрицательный знак ТКР), и при температуре 450 - 500 С существуют только очень разбавленные водные растворы этой соли, но при давлениях 750 и ЮООкГ / сж2 изобары направлены вправо ( положительный знак ТКР), и при тех же температурах 450 - 500 С существуют уже высококонцентрированные растворы, содержащие 50 - 70 вес. [22]
 |
Схематическое изображение кривых р-х Ац. я установления концентрации и давления пара насыщенных растворов в системах 1-го типа. [23] |
На этих же рисунках для пояснения сущности получаемых при эксперименте данных изображены также кривые давления пара насыщенных растворов ( кривые растворимости), изотермы и изобары растворимости. [24]
Относительно системы ванадий - водород имеются несколько разноречивые данные. Изотермы и изобары растворимости изучены вплоть до 1100 [264, 338]; ниже 400 равновесие практически не достигается, а это не позволяет подтвердить существование при низких температурах определенного гидрида. [25]
Методом кривых заряжения исследована сорбция водорода дисперсными палладий-рутениевыми сплавами, содержащими 2, 5, 7, 9, 13, 16 и 20 % ат. Получены изотермы и изобары растворимости водорода. Растворимость водорода уменьшается с увеличением содержания рутения в сплаве, достигая нуля вблизи состава, содержащего 20 % ат. Гетерогенное растворение водорода заканчивается приблизительно при содержании 13 % ат. В области сосуществования двух фаз рутений в системе Pd-Ru - Н ведет себя как четырехвалентный. [26]
Они образуют семейство изобар растворимости SiOa в воде, закономерно огибающих кривые насыщенных растворов SiOa в жидкой и паровой фазах. [27]
 |
Растворимость водорода в железе и никеле ц зависимости от температуры ( рн. 1 013 - Ш5 Па. [28] |
Тем не менее с водородом эти металлы образуют твердые растворы внедрения, концентрация водорода в которых зависит от фазовых превращений: водород значительно растворяется в жидких металлах ( Ni), причем с повышением температуры его растворимость сначала растет, а затем падает, приближаясь к нулю при температуре кипения. На рис. 183 приведены изобары растворимости для железа и никеля. [29]
 |
Изменение растворимости водорода в металлах при кристаллизации.| Изобара раствори-мости водорода в титане. [30] |
Страницы: 1 2 3 4