Изображение - орбиталь
Cтраница 1
Изображение орбиталей в табл. 10 дано схематически, так как плоский рисунок является проекцией некоторого объема. Формы, размеры и число орбиталей атома водорода при различном его возбуждении ( п) в дальнейшем будут широко использоваться при рассмотрении учения о химической связи. [1]
 |
Взаимное проникновение орбиталей Is, 2s, 3s. [2] |
Формы орбиталей для различных состояний электрона в атоме водорода приведены в табл. 2.6. Изображение орбиталей дано схематически, так как плоский рисунок является проекцией некоторого объема. Формы, размеры и число орбиталей атома водорода при различном его возбуждении ( п) в дальнейшем будут широко использоваться при рассмотрении учения о химической связи. [3]
Как и в случае двух аналогичных альтернативных описаний этилена ( с использованием ст, я и с использованием эквивалентных орбиталей), изображения орбиталей диборана могут вводить в заблуждение, так как может показаться, что в описании Пит-цера заряд сконцентрирован между ядрами бора ( в результате образования а-связи), а в случае банановых орбиталей он сосредоточен в стороне от оси бор - бор. Это кажущееся различие возникает вследствие слишком большого упрощения изображений орбиталей; на самом деле распределения заряда возникают из одинаковых волновых функций, и поэтому они идентичны. Описание образования связей в диборане с помощью трехцентровой орбитали, вероятно, предпочтительнее описания по модели про-тонированной двойной связи, особенно из-за того, что трехцент-ровую орбиталь можно рассматривать как часть многоцентровой делокализованной молекулярной орбитали. [4]
 |
Орбитали центрального атома и отвечающие им по симметрии сочетания орбиталей лигандов. [5] |
На рис. 216, а 6 показаны возможные комбинации; т-типа валентных орбиталей центрального атома и отвечающие им по симметрии сочетания орбиталей лигандов. Если совместить изображения соответствующей орбитали центрального атома и изображение орбиталей лигандов, то возникает картина их перекрывания. [6]
На рис. 212, а, б показаны возможные комбинации а-тнпа валентных орбиталей центрального атома и отвечающие им по снимет - рии сочетания орбиталей лигандов. Если совместить изображения соответствующей орбитали центрального атома и изображение орбиталей лигандов, то возникает картина их перекрывания. Как видно, на рис. 212, s - орбиталь ком-плексообразователя благодаря сферической симметрии одинаково перекрывается с орбиталями каждого из шести лигандов, расположенных по осям октаэдра. [7]
На рис. 74 показаны возможные комбинации а-типа валентных орбиталей центрального атома и отвечающие им по симметрии сочетания орбиталей лигандов. Если совместить изображения соответствующей орбитали центрального атома и изображение орбиталей лигандов, то возникает картина их перекрывания. Как видно на рис. 74, s - op - биталь комплексообразователя благодаря сферической симметрии одинаково перекрывается с орбиталями каждого из шести лигандов, расположенных по осям октаэдра. [9]
Как и в случае двух аналогичных альтернативных описаний этилена ( с использованием ст, я и с использованием эквивалентных орбиталей), изображения орбиталей диборана могут вводить в заблуждение, так как может показаться, что в описании Пит-цера заряд сконцентрирован между ядрами бора ( в результате образования а-связи), а в случае банановых орбиталей он сосредоточен в стороне от оси бор - бор. Это кажущееся различие возникает вследствие слишком большого упрощения изображений орбиталей; на самом деле распределения заряда возникают из одинаковых волновых функций, и поэтому они идентичны. Описание образования связей в диборане с помощью трехцентровой орбитали, вероятно, предпочтительнее описания по модели про-тонированной двойной связи, особенно из-за того, что трехцент-ровую орбиталь можно рассматривать как часть многоцентровой делокализованной молекулярной орбитали. [10]
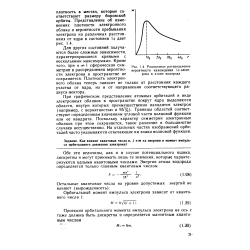 |
Радиальное распределение вероятности нахождения Is-электрона в атоме водорода. [11] |
Границы областей соответствуют определенным значениям угловой части волновой функции или ее квадрата. Поскольку характер симметрии электронных облаков при этом сохраняется, такое различие в большинстве случаев несущественно. На отдельных частях изображений орбиталей часто указываются отвечающие им знаки волновой функции. [12]
 |
Контуры радиальных волновых функций для 2s - и 2р - орбиталей атома водорода в плоскости хг. [13] |
На рис. 3.2 и 3.3 приведены угловые функции, на рис. 34 - радиальные функции. К сожалению, в рамках трехмерного пространства это невозможно Поэтому для изображения орбиталей приняты такие же диаграммы, как на рис. 3.2 и 3.3. Еще чаще дают просто сечение этих орбиталей в плоскости, проходящей через ядро. Такие сечения приведены на рис. 3.5. Существует и другая возможность состоящая в изображении контурных поверхностей волновой функции. Вначале подставим в выражение (3.11) определенные значения г, ft, р и найдем соответствующие значения волновой функции. Вычислив ф ( г Ф ф) для большого числа значений переменных, представим контурные поверхности в трехмерном пространстве, причем каждая поверхность будет являться совокупностью точек с одним и тем же значением г з ( г, О Ф) Далее удобно взять подходящее сечение контурных поверхностей Такие сечения показаны на рис. 3.6. Еще один тип представления орбиталей, который часто используют в книгах и при обсуждении химических проблем, приведен на рис. 3.7. Такие диаграммы не имеют четкой теоретической основы, но обладают тем преимуществом, что их легко можно представить графически и что они позволяют создать общую картину узловых поверхностей для данной орбитали. [14]
На рис. 3.2 и 3.3 приведены угловые функции, на рис. 3.4 - радиальные функции. К сожалению, в рамках трехмерного пространства это невозможно. Поэтому для изображения орбиталей приняты такие же диаграммы, как на рис. 3.2 и 3.3. Еще чаще дают просто сечение этих орбиталей в плоскости, проходящей через ядро. Такие сечения приведены на рис. 3.5. Существует и другая возможность, со-стоящая в изображении контурных поверхностей волновой функции. Вначале подставим в выражение (3.11) определенные значения г, О, ф и найдем соответствующие значения волновой функции. Далее удобно взять подходящее сечение контурных поверхностей. Такие сечения показаны на рис. 3.6. Еще один тип представления орбиталей, который часто используют в книгах и при обсуждении химических проблем, приведен на рис. 3.7. Такие диаграммы не имеют четкой теоретической основы, но обладают тем преимуществом, что их легко можно представить графиче ски и что они позволяют создать общую картину узловых поверхностей для данной орбитали. [15]
Страницы: 1 2
