Электростатическое воздействие
Cтраница 3
Центральный ион рассматривают с учетом его электронного строения и тех изменений, которые вносят лиганды своим электростатическим воздействием. При этом лиганды рассматриваются только как носители определенного заряда, их собственную электронную структуру не учитывают. [31]
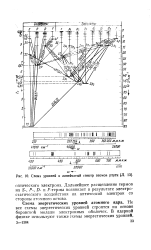 |
Схема уровней и линейчатый спектр атомов ртути Л. 13 ]. [32] |
Дальнейшее расщепление термов на S -, Р -, D - и F-термы возникает в результате электростатического воздействия на оптический электрон со стороны атомного остова. [33]
Электромерный эффект - поляризация сопряженной системы связей исходной реагирующей молекулы или иона в переходном состоянии под влиянием электростатического воздействия реагентов-партнеров по реакции с данной молекулой или ионом. [34]
Это означает, что водородные связи для Ве2 и А13 сильнее, чем для Zr4 и Hf4, хотя электростатическое воздействие поля последних катионов на протоны молекул воды больше. Объясняется это тем, что в силу исключительной малости радиусов ионов Ве2 и А13 они могут весьма близко подходить к неподеленной паре электронов молекул воды и притягивать их своим сильным электростатическим полем. Вероятно, неподеленная пара электронов молекул воды взаимодействует с незанятыми орбиталями ионов Ве2 и А13, причем это взаимодействие имеет ковалентньщ характер. В случае Ве2 доступными для него являются 2s - и 2 / о-орбитали, в случае А13 - 3s -, Зр - и Sd-орбитали. Соответственно ионы Ве2 и А13 значительно сильнее увеличивают донорную способность к образованию водородной связи ОН-групп молекул гидратной воды, чем ионы Hf4 и Zr4, что приводит к более сильным водородным связям и большему наблюдаемому сдвигу максимума полосы воды. [35]
Самое же сжатие диффузного слоя ( иначе - - уменьшение толщины подвижной ионной атмосферы вокруг гранулы) происходит под электростатическим воздействием ионов электролита-коагулятора и тем большим, чем больше концентрация последнего. Пользуясь сложным математическим аппаратом теории Дебая - Гюккеля, Мюллер достаточно убедительно обосновывает зависимость снижения С-потенциала от концентрации прибавленного электролита ( его порога концентрации), в частности, объясняет и правило Шульце-Гарди. [36]
 |
Гидратные структуры при низкой степени гидратации. [37] |
В случае ионов щелочных металлов полоса ОН-колебаний молекул воды практически не смещается в сторону меньших волновых чисел по мере возрастания электростатического воздействия поля катиона на протоны молекул воды. [38]
Это означает, что водородная связь в присутствии Се3 и La3 сильнее, чем в присутствии Mg2, несмотря на то что электростатическое воздействие на протон молекулы воды для первых двух ионов слабее. Следовательно, рассматриваемое выше взаимодействие не может быть единственной причиной увеличения донорной способности к образованию водородной связи и сдвига полосы ОН-валентных колебаний молекул воды, участвующих в водородной связи. Сдвиг полосы отражает, по-видимому, ковалентный характер взаимодействия между катионом и водой, под влиянием которого меняется также структура молекул воды. Взаимодействие такого типа легко обнаружить, поскольку оно связано с переносом неспаренных электронов молекулы воды на частично заполненные d - орбитали катиона. В катионах Се3 и La3 доступными для ковалентных взаимодействий являются 4f - и Srf-орбитали. [39]
Притяжение между твердыми частицами возникает у мелкодисперсных порошков за счет молекулярного взаимодействия контактирующих твердых поверхностей ( силы Ван-дер - Ваальса) или электростатического воздействия. Особенно заметны они при взаимодействии свежесколотых поверхностей - сразу же после проведения тонкого размола. При движении частиц вследствие их трения возникают электростатические заряды, величина которых зависит от свойств материала, условий гранулирования и отвода электричества. [40]
Метод МО дает возможность показать, что расщепление уровней d - электронов и существование высокоспиновых и низкоспиновых комплексов данного металла может происходить не только под влиянием электростатических воздействий, но и при образовании химических связей. [41]
В присутствии ионов переходных металлов водородная связь гидратной воды с анионами оказывается сильнее ( результат 27), чем это можно было ожидать, принимая во внимание электростатическое воздействие поля этих катионов на протоны молекул воды. Следовательно, в случае ионов переходных металлов наряду с поляризующим воздействием поля катионов на молекулы воды существует дополнительное взаимодействие между катионом и водой. Оно увеличивает донорные свойства ОН-групп молекул гидратной воды и сдвигает полосу ОН-валентных колебаний в направлении меньших волновых чисел. [42]
Следовательно, из диаграммы молекулярных орбиталей видно, что уровни Tig и Eg отвечают главным образом орбиталям атома металла и расщепляются ( качественно) так, как это должно происходить от чисто электростатического воздействия в теории кристаллического поля. Кроме того, в теории кристаллического поля расщепление возникает только от электростатического воздействия и требований симметрии, в то время как в теории молекулярных орбиталей расщепление происходит от кова-лентного связывания и требований симметрии. [43]
По определению электростатическое действие анода эквивалентного диода на катод должно быть одинаковым с суммарным электростатическим воздействием анода и сетки триода на катод. Электростатическое воздействие одного электрода на другой определяется наводимым на этом электроде зарядом. [44]
Для Fe, Zn, Al, Sn, Pb и других неблагородных металлов характерно WK. Вследствие электростатического воздействия соответствующее им число электронов в металле выстраивается также около поверхности, образуя отрицательный слой электричества. [45]
Страницы: 1 2 3 4