Суммарное химическое уравнение
Cтраница 1
Суммарные химические уравнения не отображают действительного хода химических реакций, а характеризуют лишь начальное н конечное состояние системы. Изучение действительного хода реально наблюдаемых химических процессов и их механизма имеет не только познавательный интерес, но н практическое значение, так как позволяет найти пути увеличения скорости и выхода нужных предметов. [1]
Известно, что суммарные химические уравнения не отображают действительного хода реакций, а характеризуют лишь начальное и конечное состояния системы. Изучение действительного хода реально наблюдаемых процессов, их механизма имеет не только познавательный интерес, но и практическое значение, так как позволяет найти пути увеличения скорости реакции и выхода нужных продуктов. [2]
При горении пирита по суммарному химическому уравнению на 4 г-моля его выделяется 800 кг / кал. [3]
Еще не для всех форм бактериального фотосинтеза установлены суммарные химические уравнения, подобные уравнениям (3.6) и (3.7) для суммарной реакции нормального фотосинтеза. [4]
Следует отметить, что линейная независимость маршрутов не означает автоматически линейную независимость суммарных химических уравнений маршрутов. Ранг матрицы стехиометрических чисел llv s ll может оказаться больше ранга матрицы Цг / Ц и тогда линейно независимым маршрутам будут отвечать линейно зависимые суммарные химические уравнения маршрутов. [5]
Следует отметить, что линейная независимость маршрутов не означает автоматически линейную независимость суммарных химических уравнений маршрутов. Ранг матрицы стехиометрических чисел, vsr может оказаться больше ранга матрицы упг, и тогда линейно независимым маршрутам будут отвечать линейно зависимые суммарные химические уравнения маршрутов. [6]
Особенно важно определение порядка у сложных реакций, так как в данном случае по суммарному химическому уравнению совершенно невозможно определить механизм и закон протекания реакции. [7]
Следует отметить, что линейная независимость маршрутов не означает автоматически линейную независимость суммарных химических уравнений маршрутов. Ранг матрицы стехиометрических чисел, vsr может оказаться больше ранга матрицы упг, и тогда линейно независимым маршрутам будут отвечать линейно зависимые суммарные химические уравнения маршрутов. [8]
Следует отметить, что в ряде случаев базис маршрутов может не совпадать с базисом итоговых уравнений химического процесса. Ранг матрицы стехиометрических чисел может оказаться больше ранга матрицы стехиомерических коэффициентов итоговых уравнений, и тогда линейно независимым маршрутам будут отвечать линейно зависимые суммарные химические уравнения маршрутов. [9]
Следует отметить, что линейная независимость маршрутов не означает автоматически линейную независимость суммарных химических уравнений маршрутов. Ранг матрицы стехиометрических чисел llv s ll может оказаться больше ранга матрицы Цг / Ц и тогда линейно независимым маршрутам будут отвечать линейно зависимые суммарные химические уравнения маршрутов. [10]
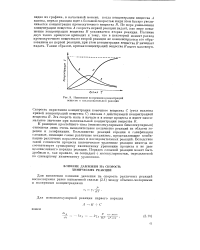 |
Изменение во времени концентраций веществ в последовательной реакции. [11] |
К реакциям простейшего типа ( мономолекулярным и бимолекулярным) относится лишь очень незначительное количество реакций из области горения и газификации. Большинство реакций горения и газификации сложные, имеющие самые различные механизмы, представляющие комбинацию различных параллельных и последовательных реакций. Вследствие такой сложности процесса кинетическое уравнение реакции никогда не соответствует суммарному химическому уравнению процесса и не дает целочисленного порядка реакции. Порядок сложной реакции может быть дробным и, как правило, не совпадает с молекулярностью, определяемой по суммарному химическому уравнению. [12]
Влияние астехиометрического компонента выражается в инициировании реакции, в изменении ее кинетики, избирательности, механизма и пр. Атомы астехиометрического компонента в отличие от атомов реагентов не входят в молекулы конечных продуктов реакции или входят без соблюдения стехиомет-рических отношений. Таким образом, эти вещества не входят в стехиометрию реакции, не фигурируют в ее суммарном химическом уравнении и являются как бы посторонними компонентами реакционной системы, почему и получили название астехиометрических. [13]
 |
Зависимость степени диссоциации СО, и Н2О от температуры парциального давления. [14] |
Порядок реакции часто бывает ниже той величины, которая получается по стехиометрическому уравнению. Это объясняется тем, что стехиометрические уравнения в большинстве случаев не вскрывают механизма реакции, а являются лишь уравнениями итогового баланса. В каждой элементарной реакции участвует не более трех атомов или молекул В силу этого суммарная зависимость порядка реакции от текущих концентраций исходных веществ часто не соответствует суммарному химическому уравнению. В частности, порядок такой реакции ( точнее порядок химического процесса в целом) может быть дрооным. [15]
Страницы: 1 2