Изомер - бутилен
Cтраница 1
Изомер бутилена удобно изобразить косо. [1]
 |
Самодельная экспериментальная препаративная газохроматогра-фическая установка ( по Алексеевой. [2] |
Изомеры бутилена обладают близкими температурами кипения, поэтому их нельзя получить в чистом виде наиболее распространенными в лабораторной практике методами ректификации. Препаративная газовая хроматография хотя и менее производительна в большинстве случаев в сравнении с ректификацией, в данном случае оказалась единственным практическим методом. [3]
 |
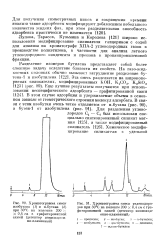
Хроматограмма трех-компонентной смеси на препаративном хроматографе. [4] |
Изомеры бутилена обладают близкими температурами кипения, поэтому их нельзя получить в чистом виде наиболее распространенными в лабораторной практике методами ректификации. Препаративная газовая хроматография хотя и менее производительна в большинстве случаев по сравнению с ректификацией, в данном случае оказалась единственным методом разделения изомеров. [5]
Соотношения изомеров бутилена, получаемых при дегидрирдвании в кипящем слое в температурном интервале 510 - 570 С, как и в неподвижном слое, остаются практически постоянными, близкими к равновесным значениям. [6]
 |
Хроматограмма смеси изобутана ( 7 и н. бутана ( 2 при 30 С на колонке 200 X X 0 4 см с графитированной сажей ( детектор нонизаципн-но-идаменньш.| Хроматограмма смеси углеводоро. [7] |
Разделение изомеров бутилена представляет собой более сложную задачу вследствие близости их свойств. В этом случае адсорбция и удерживаемые объемы в основном зависят от геометрического строения молекул адсорбата. [8]
Соотношения изомеров бутилена, получаемых при дегидрировании в кипящем слое в температурном интервале 510 - 570 С, как и в неподвижном слое, остаются практически постоянными, близкими к равновесным значениям. [9]
Известны четыре изомера бутилена; они имеют одинаковую формулу C4HS и одинаковый молекулярный вес 56 10, но обладают разными удельными весами и точками кипения, а также различными химическими свойствами. Практически всегда приходится иметь дело со смесью бутиленов. [10]
Известны четыре изомера бутилена; они имеют одинаковую формулу С4Н8 и одинаковый молекулярный вес 56 10, но обла - дают разными удельными весами и точками кипещ я, а также различными химическими свойствами. Практически всегда приходится иметь дело со смесью бутиленов. [11]
Сказанное относится также к изомерам бутилена, которые обнаруживаются только в продуктах пиролиза валина и пептидов, содержащих эту аминокислоту. Различие заключается только в том, что при пиролизе валина образуется я-бутилен, а при пиролизе пептидов гранс-2 - бутен. [12]
Поскольку состав алкилатов в случае разных изомеров бутилена сходен, предполагается, что их изомеризация происходит с высокой скоростью и состояние, близкое к равновесию, устанавливается до начала алкилирования. Этот постулат несколько отличается от ранее принятого механизма. [13]
В условиях алкилирования изопарафинов все четыре изомера бутилена претерпевают изомеризацию и полимеризуются. Эти ионные реакции протекают чрезвычайно быстро и либо предваряют алкилирование, либо сопутствуют ему. [14]
Какие соединения образуются при окислении каждого из изомеров бутилена избытком перманганата калия при нагревании. [15]
Страницы: 1 2 3