Изотерма - интенсивность - изотропное рассеяние
Cтраница 2
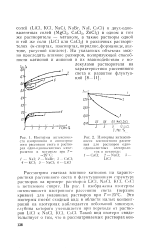
Если же взять растворы, составленные из компонентов более сильно отличающихся по размерам молекул и энергиям взаимодействия ( гептан-гексадекан, этиловый спирт-дециловый спирт), то на изотермах интенсивности изотропного рассеяния появляется широкий максимум ( рис. 3), сглаживающийся при нагревании. [16]
Интересным примером нерасслаивающихся растворов, но с заметными флюктуациями концентрации, являются спиртово-водные растворы. На рис. 5 приведены изотермы интенсивности изотропного рассеяния для растворов метанола, этанола, пропанола и бутанола в воде. Как видно, для растворов первых трех членов ряда спиртов в воде характерно наличие максимума на изотермах в области 20 - 30 мол. [18]
Рассмотрим сначала влияние катионов па характеристики рассеянного света и флуктуационпую структуру растворов па примере растворов LiCl, NaCl, KCI, CsC. Ila рис. 1 изображены изотермы интенсивности изотропного рассеяния света ( верхние кривые) для указанных растворов при Г25 С. [20]
Для выяснения роли межмолекулярного взаимодействия в развитии флюктуации концентрации рассмотрим поведение изотропного рассеяния в растворах какого-либо одного спирта, например бутанола, в различных растворителях - глицерине, бензоле, ацетоне и диоксане, размеры молекул которых близки к размерам молекул бутанола. Как видно из рис. 4, изотермы интенсивности изотропного рассеяния имеют различный вид, что, очевидно, обусловлено различным характером и интенсивностью взаимодействия между частицами раствора. [21]
На рис. 2 приведен типичный вид изотерм интенсивности изотропного рассеяния для таких систем. Как видно, для таких систем на изотермах интенсивности изотропного рассеяния вырисовывается ярко выраженный максимум, соответствующий критической концентрации, который при нагревании и удалении, таким образом, от критической температуры смешения постепенно сглаживается. Этот максимум обусловлен флкжтуациями концентрации, рассасывающимися при нагревании. [22]
Страницы: 1 2