Изотерма - лангмюр
Cтраница 2
Несмотря на широкое применение уравнений изотермы Лангмюра в практике кинетических исследований, полученные с их помощью уравнения скоростей реакций далеко не всегда приводят к однозначным результатам, особенно при значительных изменениях кинетических параметров процесса. Это объясняется тем, что ранее принятые допущения об однородности адсорбционной поверхности и отсутствии взаимодействия друг с другом хемосорбированных молекул в действительности не выполняются. Неоднородность поверхности здесь понимается в том смысле, что различные участки ее характеризуются разными теплотами хемосорбции и адсорбционными коэффициентами. При этом заполнение поверхности идет последовательно от участков с максимальными теплотами адсорбции к участкам с меньшими величинами. В соответствии с этим и теплота адсорбции Kt также будет изменяться в зависимости от доли заполнения участков с различной теплотой адсорбции на поверхности катализатора. Очевидно, что в этих условиях значение величины А / будет зависеть от изменения температуры и концентрации реагирующих веществ. Поэтому и кажущаяся энергия активации оказывается пригодной лишь для аппроксимации кинетического уравнения в некоторой ограниченной области изменения параметров процесса. [16]
Как видно из таблицы, уравнение изотермы Лангмюра может быть применено. Траубе во всех случаях, за исключением активированного угля III, где наблюдались расхождения значительно большие. [17]
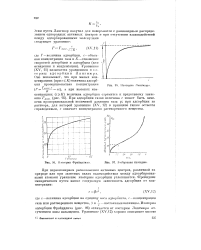 |
Изотерма Лангмюра.| Шотерма Фрейндлиха.| S-образная изотерма. [18] |
Фрейндлиха ( рис. 96) отличается от изотермы Лангмюра отсутствием зоны насыщения. [19]
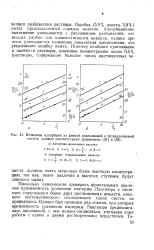 |
Величины адсорбции из смесей додекановои и тетрадекановои кислот. кривые соответствуют уравнениям ( 37 и ( 38. [20] |
Поскольку невозможно проверить фронтальным анализом применимость уравнения изотермы Лангмюра к системам, содержащим более двух растворенных веществ, никакого систематического исследования таких систем не проводилось. Однако был проведен ряд опытов, при которых применимость уравнения изотермы Лангмюра предполагалась доказанной, с чем можно согласиться, учитывая опыт работы с одним и двумя растворенными веществами. [21]
Так, Бокрис, Бломгрен и Конвей используют модифицированную изотерму Лангмюра, в которой свободная энергия адсорбции является убывающей функцией от поверхностной концентрации, но не в первой степени, как в теории Фрумкина, а в степени, отличной от единицы. [22]
Для описания межкристаллитной внутренней адсорбции примесей наряду с изотермой Лангмюра - Маклина предложены и другие виды изотерм; при этом, как правило, используют изотермы того же типа, что и при описании адсорбции на свободной поверхности. [23]
О 2 и что к каждому сорту мест применима изотерма Лангмюра. [24]
Для анализа в гомологических рядах может быть применено уравнение изотермы Лангмюра. [25]
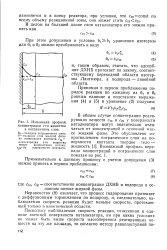 |
Изменения профиля. [26] |
ДХНБ протекает по закону, соответ-а ствующему переходной области изотермы Лангмюра, а водорода - линейной области. [27]
 |
Изотерма адсорбции сульфонола на серебристом графите. [28] |
В случае ступенчатых изотерм адсорбции к каждой ступени применимо уравнение изотермы Лангмюра. [29]
Отметим, что при со О уравнение (14.87) переходит в изотерму Лангмюра; со 0 соответствует в целом притяжению между адсорбированными атомами, а со 0 - отталкиванию. [30]
Страницы: 1 2 3 4