Изотерма - адсорбция - ленгмюр
Cтраница 1
Изотерма адсорбции Ленгмюра является основой представлений о кинетике гетерогенных реакций. Установлено, что порядок реакции зависит от степени адсорбции. [1]
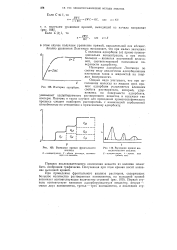 |
Изотерма адсорбции.| Выходная кривая фронтального анализа. [2] |
Изотермы адсорбции Ленгмюра по своему виду аналогичны адсорбционным изотермам газов и жидкостей на твердых поверхностях. [3]
Первоначальная изотерма адсорбции Ленгмюра была модифицирована с учетом взаимодействия соседей, подвижности с одной или двумя степенями свободы и других возможных условий и включением выражений для изменения энтропии, оцениваемых для каждого случая. [4]
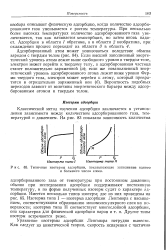 |
Типичные изотермы адсорбции, показывающие заполнение одного. [5] |
Уравнение изотермы адсорбции Ленгмюра нетрудно вывести. [6]
Уравнение изотермы адсорбции Ленгмюра применимо тогда, когда адсорбция вызывается силами, близкими по своей природе к химическим, и не осложняется побочными явлениями, например, диссоциацией молекул адсорбированного газа на поверхности. [7]
Выразите изотерму адсорбции Ленгмюра в виде уравнения, связывающего обратные величины обеих переменных, аналогично тому, как уравнение Михаэлиса - Ментен было преобразовано к виду, используемому при построении графиков Лайнуивера - Берка. [8]
Вывод уравнения изотермы адсорбции Ленгмюра для твердых адсорбентов базируется на ряде исходных предпосылок: 1) адсорбционные силы подобны силам основных валентностей и действуют на малых расстояниях; 2) адсорбционной активностью обладает не вся поверхность адсорбента, а лишь определенные активные центры, расположенные преимущественно на выпуклых участках поверхности: выступах, ребрах, углах; 3) молекулы адсорбированного газа фиксируются на адсорбционных центрах, не перемещаются по поверхности адсорбента и не взаимодействуют друг с другом. Для упрощения вывода принималось, что все адсорбционные центры энергетически равноценны и каждый такой центр может удержать только одну молекулу адсорбата. В результате такой адсорбции образуется мономолекулярный слой адсорбированных молекул. Поскольку одновременно с адсорбцией протекает обратный ей процесс десорбции, адсорбированные молекулы газа или растворенного вещества через какой-то период времени отрываются от поверхности адсорбента под действием молекулярно-кинетических сил. При равенстве скоростей этих процессов в системе устанавливается динамическое адсорбционно-десорбционное равновесие. [9]
Объединяя уравнение изотермы адсорбции Ленгмюра и уравнение Гиббса, можно получить уравнение Шишковского. [10]
Подтверждением применимости уравнения изотермы адсорбции Ленгмюра является постоянство as и экспоненциальная зависимость константы b от температуры. [11]
Это и есть уравнение изотермы адсорбции Ленгмюра. [12]
Парсонс [28] критиковал использование изотермы адсорбции Ленгмюра при рассмотрении адсорбции из растворов, поскольку она выведена для локализованной адсорбции. [13]
Это и есть уравнение изотермы адсорбции Ленгмюра. [14]
Это соотношение носит название изотермы адсорбции Ленгмюра. [15]
Страницы: 1 2 3 4