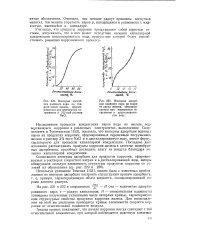
Изотерма - адсорбция - водяной пар
Cтраница 1
Изотермы адсорбции водяных паров поднимаются очень круто при низких парциальных давлениях и почти в 4 - 5 раз превышают активность силикагеля и алюмогеля при адсорбции в этих условиях. Цеолиты могут адсорбировать 19 % вес. Это свойство они сохраняют и при высоких температурах. [1]
Измерены изотермы адсорбции водяного пара глиноземом и силикагелем при температурах 0; 10; 30 С. [2]
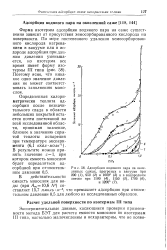 |
Адсорбция водяного пара на окисленных сажах, прогретых в вакууме при 200 ( 1, 950 ( 2 и 1000 ( 3 и в водородном потоке при 1100 ( 4, 1150 ( 5, 1700 ( б, и 3200 ( 7. [3] |
Форма изотермы адсорбции водяного пара на саже существенно зависит от присутствия хемосорбированного кислорода на поверхности. Поэтому ясно, что никакое одно значение давления не может соответствовать заполнению монослоя. [4]
Он сопоставил изотермы адсорбции водяного пара и азота на двух образцах сахарного угля ( графитированного и неграфитированного), выразив величину адсорбции в виде объема жидкого адсорбата в расчете на грамм угля. Из рис. 119 видно, что изотермы адсорбции азота относятся к изотермам I типа, а изотермы водяного пара - к изотермам V типа. [5]
Изучены [186] изотермы адсорбции водяных паров на порошке хлорида натрия. Показано, что механизм слеживания соли заключается в агрегировании частиц NaCl силами сцепления адсорбированной воды. [6]
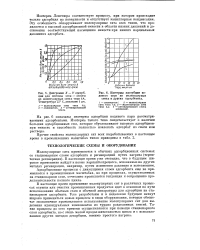 |
Диаграмма X - Y адсорбции для системы этан - этилен на молекулярных ситах типа 4А. Температура 25 С, давление i am.| Изотермы адсорбции водяного пара на молекулярных ситах и других адсорбентах. [7] |
На рис. 6 показаны изотермы адсорбции водяного пара рассматриваемыми адсорбентами. Изотерма такого типа свидетельствует о наличии больших адсорбционных сил, которые обусловливают высокую адсорбционную емкость и способность полностью извлекать адсорбат из смеси или раствора. [8]
 |
Влияние химического модифицирования поверхности сажи на адсорбцию водяных паров.| Стеклянная трубка, опущенная. [9] |
На рис. 18 представлены изотермы адсорбции водяных паров сажей. Кривая / относится к исходному образцу сажи, кривая 2 - к образцу, подвергнутому предварительно окислению с поверхности, и кривая 3 - к образцу, подвергнутому с поверхности восстановлению и графитированию. На первоначальной и в особенности на восстановленной поверхности сажи адсорбция почти не происходит, а окисленной поверхностью водяные пары адсорбируются сравнительно хорошо. [10]
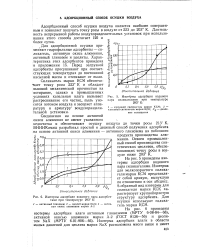 |
Изотермы адсорбции водяного.| Изотермы адсорбции водяного пара адсорбентами при температуре 293 К.. [11] |
На рис. 5 приведены изотермы адсорбции водяного пара силикагелями. Изотерма для мелкопористого силика-геля марки КСМ представляет собой кривую, выпуклую по отношению к оси абсцисс. [12]
Проведенный нами анализ большого числа изотерм адсорбции водяного пара на углеродных адсорбентах с самыми различными пористыми структурами позволяет сделать вывод, что заполнение основного объема адсорбционного пространства АУ с узкими микропорами протекает при относительном давлении Л0 55, что, по-видимому, связано со значительным эффектом наложения адсорбционных полей противоположных стенок пор. Дальнейшее увеличение размера пор до супермикропор сопровождается смещением изотерм к более высоким относительным давлениям. [13]
Адсорбционные свойства сорбентов определяются их химическим составом и характером пористой структуры, о которой для выбранных нами сорбентов можно судить по изотермам адсорбции водяного пара. [14]
Страницы: 1 2