Изотерма - адсорбция - спирт
Cтраница 1
Изотерма адсорбции спирта идет несколько выше изотермы адсорбции воды, причиной чему яшшется, очевидно, увеличение плотности спирта в адсорбированном состоянии. [1]
Приводим на рис. 6 изотермы адсорбции спиртов из неполярного вазелинового масла на стали. Впрочем, отклонения почти не выходят за пределы ошибок опыта. [2]
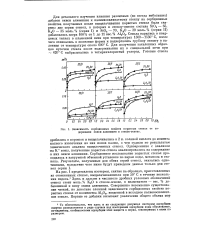 |
Зависимость сорбционных свойств пористых стекол от содержания окиси алюминия в стекле-основе. [3] |
То обстоятельство, что здесь и на следующих рисунках изотермы адсорбции спиртов располагаются в ряде случаев над изотермами адсорбции воды обусловлено, по-видимому, особенностями адсорбции этих веществ в порах, соизмеримых с ними по размерам. [4]
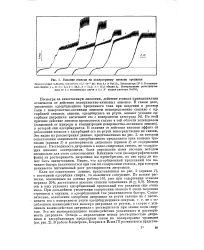 |
Влияние этанола на нолярограмму катиона тропилия. [5] |
Если же сопоставить данные, представленные на рис. 2 ( кривая 1), с изотермой адсорбции спирта, то выяснится следующее. Между тем в этих условиях адсорбционный предельный ток увеличен еще очень мало, При дальнейшем увеличении содержания этанола 8 очень медленно стремится к единице, а адсорбционный ток увеличивается быстро. Это же межмолекулярное взаимодействие увеличивает и растворимость дитропила. [6]
Молекулы спиртов отличаются от молекул воды наличием углеводе родной части, которая электрокинетически сильно притягивается к графиту. Это увеличивает взаимодействие адсорбат - адсорбент, так что изотермы адсорбции спиртов поднимаются круче изотермы адсорбции воды. Кроме того, молекулы спиртов сильно взаимодействуют друг с другом ( аде орбат - адсорбат), что приводит к образованию между их гидроксильпымигруппами водородной связи. Поэтому по мере заполнения поверхности графита рост адсорбции усиливается и поверхность сплошь покрывается пленкой: спирта, причем на мономолекулярную адсорбцию налагается полимолекулярная. На рис. 17 показано изменение изотерм адсорбции на графитированной канальной саже при переходе от воды к спиртам. По мере увеличения углеводородной части молекулы спирта занимаемая ею площадь увеличивается и соответственно уменьшается общее количество молекул, покрывающих поверхность плотным слоем. Поэтому при достаточно больших давлениях пара изотермы адсорбции разных спиртов пересекаются. [7]
На рис. 112 изображены изотермы адсорбции паров воды при 99 4 на четырех ионных адсорбентах: окиси тория, окиси алюминия, окиси вольфрама и окиси циркония. Сплошные кривые изображают объем адсорбированного газа на 1 см3 адсорбента, пунктирные кривые - адсорбированный объем на 1 0 адсорбента. На рис. 113 изображены изотермы адсорбции спирта на тех же четырех адсорбентах при тех же температурах. [8]
На рис. 112 изображены изотермы адсорбции паров воды при 99 4 на четырех ионных адсорбентах; окиси тория, окиси алюминия, окиси вольфрама и окиси циркония. Сплошные кривые изображают объем адсорбированного газа на 1 см3 адсорбента, пунктирные кривые - адсорбированный объем на 1 г адсорбента. На рис. 113 изображены изотермы адсорбции спирта на тех же четырех адсорбентах при тех же температурах. [9]
Это характерно для соединений, имеющих нулевой порядок реакции по гидрируемому веществу. Следовательно, рост скорости гидрирования определяется активацией водорода. Значительное смещение потенциала при гидрировании, особенно на никеле, приводит к быстрой дезактивации катализатора, поэтому наиболее целесообразно работать при максимальной скорости в отсутствие избытка непредельного соединения в растворе. Рост смещения потенциала при накоплении продукта реакции позволяет рассчитать изотерму адсорбции р-фенилпропиолового спирта. Проведение реакции в таком же режиме при другой температуре позволяет рассчитать температурные коэффициенты оптимальной скорости и адсорбции продукта реакции. Так, например, при гидрировании диметилэтинилкарбинола на никеле при одинаковой заданной скорости, равной 4 8 мл Н2 в 1 мин. [10]
Для перехода от гиббсовских избытков Г к поверхностным концентрациям необходимо поэтому пользоваться какой-то моделью строения пограничного слоя раствора. Применительно к границе раздела раствор - воздух поверхностные концентрации этанола рассчитывались по кривым зависимости поверхностного натяжения ( а) - от состава раствора. Согласно результатам расчетов, с ростом активности спирта в объемной фазе раствора его поверхностная концентрация быстро увеличивается до величины, близкой к предельной, а затем медленно дорастает до предельной. Однако при наиболее вероятных предположениях о величинах площадей поверхности, занимаемых молекулой спирта и воды в адсорбированном состоянии ( iSon 20 и SB 10 А2), на верхней части изотермы адсорбции спирта получался плоский минимум, который связывался с полимолекулярной адсорбцией, но ее вклад был относительно невелик. Следует заметить, что в этом случае речь идет не о плотных полимолекулярных слоях, которые, как показали Фрумкин, Городецкая и Чугунов [10] и подтвердили последующие емкостные измерения [11, 12], образуются на ртути в растворах фенола и капроновой кислоты при концентрации, близкой к насыщению, а о диффузионно построенном адсорбционном слое этанола. [11]
Молекулы спиртов отличаются от молекул воды наличием углеводе родной части, которая электрокинетически сильно притягивается к графиту. Это увеличивает взаимодействие адсорбат - адсорбент, так что изотермы адсорбции спиртов поднимаются круче изотермы адсорбции воды. Кроме того, молекулы спиртов сильно взаимодействуют друг с другом ( аде орбат - адсорбат), что приводит к образованию между их гидроксильпымигруппами водородной связи. Поэтому по мере заполнения поверхности графита рост адсорбции усиливается и поверхность сплошь покрывается пленкой: спирта, причем на мономолекулярную адсорбцию налагается полимолекулярная. На рис. 17 показано изменение изотерм адсорбции на графитированной канальной саже при переходе от воды к спиртам. По мере увеличения углеводородной части молекулы спирта занимаемая ею площадь увеличивается и соответственно уменьшается общее количество молекул, покрывающих поверхность плотным слоем. Поэтому при достаточно больших давлениях пара изотермы адсорбции разных спиртов пересекаются. [12]
Страницы: 1