Изотерма - адсорбция - двуокись - углерод
Cтраница 1
Изотермы адсорбции двуокиси углерода кусковым силикагелем КСМ при температурах от 163 до 123 К и давлениях воздуха от 0 1 до 14 5 Мн / м показаны на рис. 2, где статическая емкость выражена в кубических сантиметрах СО2 ( при температуре 293 К и давлении 760 мм рт. ст.) на 1 г адсорбента. Ход изотерм показывает, что с повышением давления воздуха емкость адсорбента вначале возрастает, проходит через максимуму а затем уменьшается и при давлениях выше 12 5 Мн / м2 остается практически постоянной. [1]
Изотермы адсорбции двуокиси углерода из сжатого атмосферного воздуха, содержащего 0 03 % СО2, определялись на установке, схема которой показана на фиг. [2]
Изотермы адсорбции двуокиси углерода при 20 на опытных гранулированных образцах цеолита NaA, полученных нами от Б. А. Липкинда и Я. В. Мирского ( рис. 3), поднимаются в начальной области менее круто. [3]
Изотермы адсорбции двуокиси углерода кусковым силикагелем КСМ при температур ах от - 110 до - 150JC и давлениях воздуха от 1 до 145 ата показаны на фиг. [4]
Определены изотермы адсорбции двуокиси углерода из сжатого атмосферного воздуха, содержащего 0 03 % СС2, при температуре 20 С промышленными образцами цеолитов СаА и NaX. Полученные величины статической емкости указывают на целесообразность их использования для адсорбционной очистки воздуха высокого давления от COz при положительных температурах. [5]
На рис. 26 приведен ряд изотерм адсорбции двуокиси углерода на активированном угле при различных температурах. [6]
Магнус, Заутер и Кратц [95], исследуя адсорбцию двуокиси углерода углем, получили данные для дифференциальных теплот адсорбции двуокиси углерода на очищенном угле, указывающие, что эти теплоты постоянны в области низких давлений ( до 3 мм); они считали, что это объясняется удалением примешанной окиси. Оказалось, что изотерма адсорбции двуокиси углерода получена наложением изотермы адсорбции двуокиси углерода на изотерму адсорбции примешанной к ней окиси. Теплота адсорбции двуокиси углерода на чистом угле лежит между 7000 и 8000 кал, в то время как теплота сорбции двуокиси углерода с примесью окиси углерода порядка 20 000 и 30 000 кал. Заутер [125] считал вероятным, что высокие теплоты адсорбции, особенно дифференциальные теплоты, могут служить доказательством того, что происходит скорее химическая сорбция, чем чистая адсорбция. Устойчивые поверхностные соединения образуются с выделением большого количества энергии. МакКи [101] и Маршалл и Брамстон-Кук [97] также обратили внимание на то, что теплота адсорбции кислорода изменяется вследствие химической реакции между кислородом и углем. [7]
Магнус, Заутер и Кратц [95], исследуя адсорбцию двуокиси углерода углем, получили данные для дифференциальных теплот адсорбции двуокиси углерода на очищенном угле, указывающие, что эти теплоты постоянны в области низких давлений ( до 3 мм); они считали, что это объясняется удалением примешанной окиси. Оказалось, что изотерма адсорбции двуокиси углерода получена наложением изотермы адсорбции двуокиси углерода на изотерму адсорбции примешанной к ней окиси. Теплота адсорбции двуокиси углерода на чистом угле лежит между 7000 и 8000 кал, в то время как теплота сорбции двуокиси углерода с примесью окиси углерода порядка 20 000 и 30 000 кал. Заутер [125] считал вероятным, что высокие теплоты адсорбции, особенно дифференциальные теплоты, могут служить доказательством того, что происходит скорее химическая сорбция, чем чистая адсорбция. Устойчивые поверхностные соединения образуются с выделением большого количества энергии. МакКи [101] и Маршалл и Брамстон-Кук [97] также обратили внимание на то, что теплота адсорбции кислорода изменяется вследствие химической реакции между кислородом и углем. [8]
Как видно из рисунка, в этом случае получаются вполне удовлетворительные прямые. При более высоких величинах адсорбции экспериментальные точки отклоняются от прямых линий, что и следовало ожидать на основании развитых выше соображений. Исходя из своей теории, Вильяме вычислил удельные поверхности для углей, с которыми производили измерения Гомфрей [2] и Титов [1], и получил 130 м2 / г и соответственно 800 м г. По изотерме адсорбции аргона при - 190, измеренной Гомфрей, и по изотерме адсорбции двуокиси углерода при - 76 5, найденной Титовым, можно установить, что удельная поверхность первого угля составляла около 420 м2 / г, а второго - около 550 л 2 / г. Проведенное Вильямсом вычисление удельной поверхности угля, с которым работал Титов, является весьма мало надежным, однако данные Гомфрей позволяют провести довольно точное вычисление на основе его теории. Однако значения vm, вычисленные из обоих этих уравнений, соответствуют насыщению не всей поверхности, а только некоторой ее части, для которой q приближенно постоянно. Оба уравнения могут соблюдаться даже и в том случае, если q изменяется вдоль поверхности, при условии, что изменения q компенсируются противоположными изменениями fa ( T) в уравнении ( 35) таким образом, чтобы Ь оставалось приближенно постоянным. [9]
Как видно из рисунка, в этом случае получаются вполне удовлетворительные прямые. При более высоких величинах адсорбции экспериментальные точки отклоняются от прямых линий, что и следовало ожидать на основании развитых выше соображений. Исходя из своей теории, Вильяме вычислил удельные поверхности для углей, с которыми производили измерения Гомфрей [2] и Титов [ ], и получил 130 м2 / г и соответственно 800 м2 / г. По изотерме адсорбции аргона при - 190, измеренной Гомфрей, и по изотерме адсорбции двуокиси углерода при - 76 5, найденной Титовым, можно установить, что удельная поверхность первого угля составляла около 420 м / г, а второго - около 550 м2 / г. Проведенное Вильямсом вычисление удельной поверхности угля, с которым работал Титов, является весьма мало надежным, однако данные Гомфрей позволяют провести довольно точное вычисление на основе его теории. Однако значения vm вычисленные из обоих этих уравнений, соответствуют насыщению не всей поверхности, а только некоторой ее части, для которой q приближенно постоянно. Оба уравнения могут соблюдаться даже и в том случае, если q изменяется вдоль поверхности, при условии, что изменения q компенсируются противоположными изменениями fa ( T) в уравнении ( 35) таким образом, чтобы Ъ оставалось приближенно постоянным. [10]
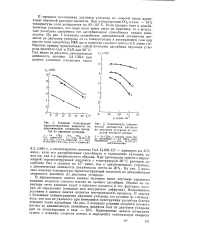 |
Зависимость динамической активности цеолитов по двуокиси углерода от скорости газового потока. [11] |
В процессе поглощения двуокиси углерода из газовой смеси происходит заметный разогрев цеолитов. При концентрации С02 в газе - 10 % температура слоя повышается на 40 - 50 С. Если процесс идет в адиабатических условиях, что чаще всего имеет место на практике, то в результате разогрева адсорбента его адсорбционная способность сильно понижается. На рис. 1 показана зависимость динамической активности цеолитов по двуокиси углерода от ее концентрации в поступающем газе при высоте слоя адсорбента 1000 мм и скорости газового потока 0.6 л / мин. Верхние кривые представляют собой изотермы адсорбции двуокиси углерода цеолитов СаА и NaX при 20 С. [12]
Страницы: 1