Полная изотерма
Cтраница 2
Если установка с капиллярной бюреткой предназначена как для подробного изучения начальных участков изотерм, так и для измерения полных изотерм до p / ps, то полезно установить две капиллярные микробюретки различного диаметра. [16]
 |
Зависимость иредэкспоненциальной функции ф ( ( У, Т, / о от напряжения при rconst и. [17] |
В интервале напряжений, включающем границы [ о0 ок ], уравнение (6.15) при Tconst в координатах Igt-с дает полную изотерму долговечности. [18]
Метод после адсорбции дает возможность экспериментально выделить для исследования отдельные, особо интересные участки изотермы из большой области концентраций или же определить полную изотерму в виде отдельных отрезков. [19]
Сравнение теории с экспериментом проводилось в этой главе в основном для ПММА ( неориентированный) и для капронового волокна ( ориентированный полимер), для которых рассчитаны Ос, Оф и ок и построена полная изотерма долговечности. Для сильно дефектных образцов с макротрещинами предложены соответствующие уравнения долговечности. [20]
Компонент с максимальной температурой - это тот компонент, который начинает плавиться первым. Полные изотермы могут быть построены путем графического изображения в виде пересекающихся линий результатов серии таких расчетов. На рисунках к примеру 8.8 впадины невелики, а на рисунках к примеру 8.9 отчетливо выражены. [22]
Изложенная термофлуктуа-ционная теория прочности основана на двухуровневой модели разрыва химических связей в вершине микротрещины и из нее следует существование безопасного сто и критического ск напряжений, являющихся границами действия термофлуктуаци-онного механизма разрушения. Полная изотерма долговечности т ( ст) при ст - ст0 предсказывает т - х, а при 0юо - линейный участок в координатах Igr-а вплоть до напряжения Тф, при котором происходит переход от термофлуктуационного механизма разрушения к атермическому. При а0ф основным вкладом в долговечность т является атермический вклад тк, лежащий в микросекундном диапазоне времени. [23]
Графическое изображение и их анализ также подобны ( см. рис. III. Таким образом, полная изотерма ионного обмена должна быть представлена поверхностью ОВВ О ( см. рис. 111.26), ширина которой ( координата 00) соответствует обшей ионной концентрации раствора. Уравнение (111.152) отражает сечение поверхности изотермы при данной обшей ионной концентрации раствора. В зависимости от последней несколько изменяется коэффициент обмена. [24]
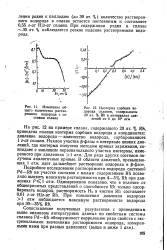 |
Изотерма сорбции водорода сплавом, содержащим 20 ат. % Rh в интервалах-дав-лений от 0 до 104 атм.| Изменение общего количества растворенного водорода с составом сплава. [25] |
Rh, приведена полная изотерма сорбции водорода в координатах: давление водорода - количество водорода, сорбированного 1 г-ат сплава. Наклон участка р-фазы в интервале низких давлений, где изотерма получена методом кривых заряжения, совпадает с наклоном первоначального участка изотермы, измеренного при давлениях 1 атм. Для ряда других составов получены аналогичные кривые. В области давлений, превышающих 1 атм, идет дальнейшее растворение водорода в р-фазе. [26]
Итак, степенная изотерма адсорбции должна быть выполнима в области средних заполнений поверхности. Как и в случае логарифмической изотермы, уравнение данной изотермы может рассматриваться как приближенное выражение уравнения полной изотермы для всего интервала адсорбции. [27]
 |
Схема сорбтометра. [28] |
По величинам Fdes Fads и р определяют первую точку изотермы БЭТ. Повторные измерения при различных соотношениях He / N2 и вычисление соответствующих значений Fdes и Р позволяют начертить полную изотерму БЭТ. [29]
 |
Схема сорбтометра. [30] |
Страницы: 1 2 3
