Изотоп - йод
Cтраница 1
Изотоп йода собирают центрифугированием на целлофановой пленке. Синтез йодистого - J128 этила проводят в колбе емкостью 2 мл с боковым отростком для введения пленки с йодом и фосфора. Спирт добавляют по внутренней трубке с краном. Окраска йода исчезает через 5 - 10 мин. [1]
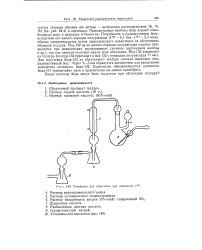 |
Установка для перегонки при отделении J131. [2] |
Какие изотопы йода могут быть получены при облучении теллура. [3]
Краткий период полураспада изотопа йода ( 8 суток) ограничивает возможности химического синтеза. Ряд соединений может быть получен только методом изотопного обмена. Этим методом получены: тиопентал натрия S35, тпоуксусная кислота - S35 и ее эфиры, тиомочевина. [4]
В природе встречается один изотоп йода зз. Йод накопляется в морской воде ( до 2 мг на 1 л), из которой его извлекают некоторые водоросли. Организм, получая йод с пищей, накапливает его в щитовидной железе. Недостаток йода вызывает заболевание. [5]
При делении урана образуется ряд изотопов йода ( табл. 2), многие из которых нашли применение в медицине. Йод-131 получают также облучением нейтронами соединений теллура [11 - 12], изотопы же J132 и J133 выделяют только из продуктов деления. [6]
Для получения раствора с требуемой концентрацией навеску изотопа йода растворяют в пиридине и объем полученного раствора доводят пиридином до определенного объема. Аликвотные пробы этого раствора объемом 1 мл переносят в колбы Эрлен-мейера с пришлифованной пробкой, в каждой из которых находится раствор 100 мг однозарядного положительного комплекса йода с пиридином ( примечание 2) в 4 мл пиридина. После тщательного перемешивания часть растворов помещают в термостат с температурой 26 3; из остальных растворов комплекс тотчас же вытесняют обработкой петролейным эфиром. [7]
Как видно из таблицы, среди обследованных рабочих имеет место повышение поглощения изотопа йода, что свидетельствует об усилении активности щитовидной железы. [8]
В зависимости от продолжительности облучения урана и его выдержки после извлечения из реактора в продуктах деления преобладает тот или иной изотоп йода. Йод-132 получают по мере необходимости из Те182, выделенного на носителе Те из продуктов деления. Для получения J133 порцию U30g, облученную в течение 24 ч, растворяют в H3S04 FL02 и продувкой азотом извлекают из раствора йод. [9]
Один из них, кобальт-60, дает высокоэнергетическое гамма-излучение и стоит намного дешевле радия, другой - один из изотопов йода, - при приеме его раствора внутрь, накапливается в щитовидной железе, где разрушает раковые клетки. Однако толерантность Организма к радиации Ограничена, и всегда существует опасность, что облучение в большей степени будет способствовать возникновению опухоли, нежели уничтожать ее. [10]
Доза внешнего облучения всего тела от загрязненного воздуха в помещениях АС или от проходящего облака на местности будет примерно в 100 раз меньше, чем доза облучения щитовидной железы от ингаляции изотопов йода. Легкие становятся критически облучаемым органом в тех случаях, когда доза на щитовидную железу от ингаляции радиоизотопов йода существенно снижена профилактическим приемом препаратов стабильного йода. [11]
Здесь звездочкой отмечено возбужденное состояние ядра. Для разделения изотопов йода 1271 и 1281 в качестве мишени используется йодистый этил. [12]
В первые дни после аварии наиболее опасны радиоактивные изотопы йода, которые накапливаются щитовидной железой. Наибольшая концентрация изотопов йода обнаруживается в молоке, что особенно опасно для детей. [13]
Закон распада радиоактивного вещества состоит в том, что скорость распада пропорциональна наличному количеству вещества. Известно, что период полураспада изотопа йода Ji3i равен 8 суток. [14]
Метод сходен с методом Сэнджера, а химизм реакции уже излагался выше ( см. гл. Особенность этого метода состоит в том, что пипсилхло-рид метят изотопом йода, и пипсилпроизводные аминокислот после хроматографического разделения определяют радиометрически. Результаты анализа обычно хорошо согласуются с данными, получаемыми динитрофторбензольным методом. Недостаток этого метода по сравнению с динитрофторбензольным состоит в том, что некоторые N-концевые группы, если они глубоко внедрены в молекулу белка, могут оказаться недоступными для пипсил-хлорида, но доступными для динитрофторбензола. Поэтому этот прием анализа N-концевых аминокислот используется реже. [15]
Страницы: 1 2