Тяжелые изотоп
Cтраница 2
Впрочем, получить сравнительно долгоживущие тяжелые изотопы 107-го элемента еще предстоит. [16]
Хотя отдельные ядра тяжелых изотопов могут делиться самопроизвольно, вероятность такого деления крайне мала. Поэтому обычно процесс деления вызывают, облучая вещество потоками дейтронов, протонов, а-частиц высокой энергии. Однако практическое значение имеет лишь деление ядер иод действием нейтронов. [17]
Из-за малого содержания тяжелых изотопов в исходном кислороде концентрирование требовало много времени: за 1 / 2 года было получено 250 см3 концентрата. Выделение 99 % молекул 0 ] s cl % 017018 оказалось возможным потому, что на горячей платиновой проволоке трубки по мере концентрирования поддерживалось равновесие согласно реакциям О 6 0 8 2016018и О 6 О 2016017, благодаря которым легкие изотопы отделялись от тяжелого. За 5 месяцев было получено 1 5 л этого концентрата. [18]
Из-за малого содержания тяжелых изотопов в исходном кислороде концентрирование требовало много времени: за 1V2 года было получено 250 см3 концентрата. [19]
Было изучено влияние тяжелых изотопов, входящих в состав молекулы, на образование осколочных ионов в масс-спектре. Ошибки могут возникнуть, если для измерения относительного содержания изотопов используются осколочные ионы, обладающие различной эффективностью образования. Для CH3D и СН4 вероятность отрыва атома дейтерия при ионизации составляет лишь 0 38 от вероятности ионизации водорода. [20]
 |
Известные в настоящее время трансурановые элементы. [21] |
Основными процессами распада наиболее тяжелых изотопов являются а-распад и спонтанное деление. Так, у изотопа фермия 100Fm256 период полураспада по отношению к спонтанному делению равен 2 7 ч, а изотоп курчатовия Ю4 Ки260 имеет ГСПонт. Из последней графы этой таблицы видно, что периоды полураспада изотопов трансурановых элементов в среднем резко падают с увеличением Z, Это уменьшение времени жизни, казалось бы, кладет естественный предел возможности получения новых элементов: при каком-то Z окажется, что все изотопы практически мгновенно распадаются, так что их синтез и исследование станут невозможными. [22]
Путем химического обмена содержание тяжелых изотопов может быть увеличено. [23]
Удаление избытка одного из тяжелых изотопов может быть достигнуто разными способами. Часто применяют вымывание дейтерия длительным пропусканием через анализируемую воду аммиака или сернистого водорода. Обменная изотопная реакция их водорода с дейтерием воды ведет к удалению последнего. Таким же образом может быть удален избыточный тяжелый кислород пропусканием избытка двуокиси углерода или двуокиси серы через анализируемую воду. Удаление избыточного дейтерия может быть достигнуто также тем, что парами анализируемой воды окисляют медные стружки при высокой температуре, а затем восстанавливают полученную окись меди водородом нормального изотопного состава. Это дает воду, вся избыточная плотность которой обязана тяжелому кислороду первоначальной воды. Возможны разнообразные другие видоизменения этих способов. [24]
Предположим, что в отсутствие тяжелых изотопов это соединение образовало интенсивный пик ионов с массой 199 ( CioH15O4), который в десять раз больше молекулярного. [25]
Большая привлекательность центрифуг в разделении тяжелых изотопов, таких как изотопы урана, состоит в том, что, в отличие от газовой диффузии, коэффициент разделения зависит не от квадратного корня из отношения масс, а от разности масс двух изотопов. [26]
Среди легких элементов меньшую распространенность имеют тяжелые изотопы, а у тяжелых элементов меньшую распространенность имеют изотопы легкие. Последнее обстоятельство имеет следствием то, что центробежному методу часто приходится иметь дело с малораспространенными изотопами, такими как 124Хе и 126Хе, 112Sn, 123Te и др. Обогащать легкие изотопы на каскадах центрифуг сложнее, чем тяжелые, из-за влияния на процесс легких примесей. [27]
Не всегда, однако, молекулы тяжелых изотопов менее летучи, чем молекулы легких изотопов. Некоторые вещества обладают необычайно высокой упругостью пара при комнатной температуре. В большинстве случаев эти вещества находятся в ассоциированной форме. Таким примером является Н2О и HDO, отношение упругостей пара которых при температуре 313 К составляет 1 059 [1120], и разделение их методом перегонки наиболее целесообразно. Бревер и Мадорский [268] описали 10-ступенчатый молекулярный куб с противотоком для разделения изотопов ртутк. [28]
Если дано общее содержание дейтерия и тяжелых изотопов кислорода в воде, то легко вычислить концентрации всех ее изотопных разновидностей. [29]
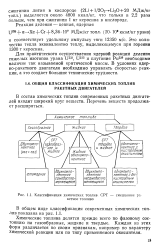 |
Классификация химических топлив. СРТ - смешанное ракетное топливо. [30] |
Страницы: 1 2 3 4