Тяжелые изотоп - водород
Cтраница 2
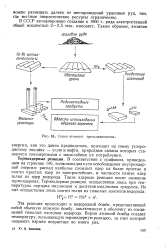 |
Схема атомной промышленности. [16] |
Эта реакция происходит в водородной бомбе, представляющей собой обычную атомную бомбу, заключенную в оболочку из соединений тяжелых изотопов водорода. Взрыв атомной бомбы создает температуру, вызывающую термоядерную реакцию, за счет которой мощность взрыва возрастает во много раз. [17]
Неучастие хлорофилла в переносе протона ( вариант За) объясняет упомянутые выше наблюдения, по которым в него не входят тяжелые изотопы водорода при ведении фотосинтеза в дейтерийной или тритиевой воде. [18]
Важный шаг в этой области был сделан Шенхеймером и его сотрудниками из Колумбийского университета в тридцатых годах, когда стали доступны тяжелые изотопы водорода и азота в количествах, достаточных для синтеза меченых аминокислот и жирных кислот. Дейтерий и 15N нерадиоактивны, но их можно обнаружить при помощи прибора, называемого масс-спектрометром. Изотопы в газообразных пробах разделяются в магнитном поле прибора, после чего можно измерить количество каждого из них. [19]
Что же следует из всего этого для решения основной проблемы - достижения условий, при которых возможна управляемая термоядерная реакция. В наиболее горючей смеси тяжелых изотопов водорода - дейтерия и трития - термоядерное пламя вспыхивает при температуре выше 50 млн град. [20]
D случае легких элементов широко пользуются точными измерениями разных физич. Для определения содержания - тяжелых изотопов водорода и кислорода в воде чаще всего применяют разные дсн-симетрпч. Наиболее точные и простые основаны па сравнении темп-р флотации кварцевого поплавка в анализируемой воде и стандарте, капель воды в нерастпоряющей ее жидкости или поплавка, наполненного исследуемой водой и погруженного в иоду природного изотопного состава. Применяют также измерение аналогичными флотационными способами плотности образца в виде кристаллика исследуемого вещества или, главным обрааом для дейтерия и ею летучих соединений, плотности газа с помощью газовых весов. Для дейтерия н его газообразных соединений хорошим н чувствительным методом служит намерение теплопроводности в разных видоизменениях манометра Ццранн. Большинство перечисленных методик можег быть применено к малым количествам анализируемой пробы, порядка мг и даже меньше. [21]
Установлено, что воды различных больших рек имеют постоянный изотопный состав. Воды же морей и океанов, как правило, содержат пусть чрезвычайно незначительное, но вполне определимое повышенное количество тяжелых изотопов водорода и кислорода. Разумеется, если бы воды морей и океанов постоянно не разбавлялись речными водами и водами атмосферных осадков, то содержание тяжелых изотопов водорода и кислорода в них постоянно увеличивалось бы. [22]
Методы определения содержания жидкости в организме основаны на изучении концентрации веществ, введенных в кровяное русло. Так, при определении общей жидкости тела вводят вещества, которые свободно проникают через эндотелий капилляров, клеточные мембраны, гематоэнцефалический барьер и равномерно распределяются во всех водных пространствах. Для этого применяют тяжелые изотопы водорода ( тритий, дейтерий), антипирин, сульфаниламиды, мочевину. [23]
Следует заметить, что распространенность тяжелых изотопов водорода ( 0 016 %) и одного из изотопов кислорода ( 17О, 0 037 %) слишком мала для точных расчетов такого рода, поскольку точность измерений интенсивностей изотопных пиков на современных спектрометрах низкого разрешения не позволяет уверенно оперировать с такими незначительными величинами. В клад атомов водорода составляет менее 0 03 этой величины, и для приблизительных оценок им можно пренебречь. [24]
Для водорода, как ни для какого другого элемента, относительное различие изотопных масс достигает значительной величины. Поэтому, хотя все изотопы характеризуются одинаковой электронной структурой, они заметно различаются не только физическими, но и химическими свойствами. Благодаря резкому преобладанию протия влияние тяжелых изотопов водорода сказывается незначительно и может быть зафиксировано лишь в очень точных экспериментах. Поэтому без большой погрешности можно считать, что свойства природного водорода соответствуют свойствам системы, состоящей из чистого протия. [25]
Способ этот, как и все другие спектральные методы количественного анализа, основанные на сравнении интенсивностей спектров, не очень точен, и в лучшем случае достоверен до нескольких процентов, но он имеет некоторые преимущества. Спектральный анализ отличается исключительной чувствительностью. Как уже указывалось, это позволило открыть существование получивших затем важное применение тяжелых изотопов водорода, углерода, азота и кислорода, содержание которых меньше того, которое могло быть в свое время обнаружено масспектрографиче-ским путем. Из спектров же были получены первые, большей частью очень приблизительные данные о пропорции этих изотопов в природных элементах. [26]
Метод изотопного разбавления может быть применен разнообразными способами для анализа сложных органических смесей. Особенно широкое распространение он начинает получать в биохимии. Работы в этом направлении были выполнены Риттенбергом и Фостером ( 1940) с применением, стабильных тяжелых изотопов водорода, углерода и азота для определения ряда аминокислот в гидролизатах гемоглобина и альбуминов, а также для определения пальмитиновой кислоты в животных жирах. Для этого-синтезировалось небольшое количество каждого из определяемых соединений, меченное тяжелым изотопом какого-либо из перечисленных элементов, и несколько миллиграммов его прибавлялось к гидролизату. [27]
Установлено, что воды различных больших рек имеют постоянный изотопный состав. Воды же морей и океанов, как правило, содержат пусть чрезвычайно незначительное, но вполне определимое повышенное количество тяжелых изотопов водорода и кислорода. Разумеется, если бы воды морей и океанов постоянно не разбавлялись речными водами и водами атмосферных осадков, то содержание тяжелых изотопов водорода и кислорода в них постоянно увеличивалось бы. [28]
В последнее время, особенно с осуществлением возможности относительно легко получать радиоактивные изотопы, все шире начали пользоваться мечеными молекулами. Для пометки обычно применяются как стабильные природные тяжелые изотопы водорода ( D), азота ( N15) кислорода ( О18) и углерода ( С13), так и искусственные радиоактивные изотопы углерода ( С14), фосфора ( Р32), серы ( S35), железа, натрия, калия и иода. [29]
В нашем курсе мы не рассматриваем строение ядер атомов и ядерные превращения. Заметим только, что число ядерных зарядов обусловлено числом протонов в ядре. Протон - это ядро легкого изотопа водорода, положительный заряд которого численно совпадает с зарядом электрона, а масса его 1 00760 у. В ядрах других атомов, в том числе в ядрах тяжелых изотопов водорода ( дейтерия и трития), есть еще нейтроны - частицы с нулевым зарядом и массой 1 00899 у. Изотопы - это атомы одного и того же химического элемента, имеющие одно и то же число протонов в ядре, но разное число нейтронов, вследствие чего массы изотопов различны, а заряды их ядер одинаковы. [30]
Страницы: 1 2 3