Установление - равновесие
Cтраница 3
Установление равновесия сопровождается изменением значения сг на границе раздела и возникновением равновесного значения Г растворенного вещества. Связь между этими двумя важнейшими параметрами, характеризующими энергию и состав слоя, можно получить путем рассмотрения системы, которая включает две объемные фазы и один поверхностный слой. [31]
Установление равновесия сопровождается изменением значения о на границе раздела и возникновением равновесного значения Г растворенного вещества. Связь между этими двумя важнейшими параметрами, характеризующими энергию и состав слоя, можно получить путем рассмотрения системы, которая включает две объемные фазы и один поверхностный слой. [32]
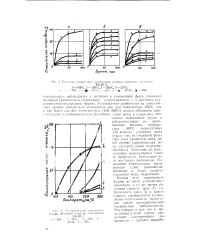 |
Кинчтика потери веса различными ионными формами катнонпта.| Те -. -. шературпан потери обменной емкости. [33] |
Установление равновесия на кинетических кривых потери веса катионитом как при температуре 100 С, так п при более высоких температурах ( 150, 200 С) можно объяснить энергетической неравноценностью различных слоев воды в гидратных оболочках ионогенных групп и нейтрализующих их проти-воионов. Видимо, температура 1 ( ЮПС недостаточна для полного удаления воды гидратации из смоляной фазы. Удаления же близлежащих молекулярных слоев не происходит, вследствие чего наступает равновесие. Повышение температуры, вызывающее сдвиг равновесия, приводит к более полному удалению воды гидратации. [34]
 |
Эбулиоскоп Шена и Шульца. [35] |
Установление равновесия между давлением паров растворителя и атмосферным давлением может происходить без видимого внешнего кипения. [36]
Установление равновесия сопровождается изменением значения о на границе раздела и возникновением равновесного значения Г растворенного вещества. Связь между этими двумя важнейшими параметрами, характеризующими энергию и состав слоя, можно получить путем рассмотрения системы, которая включает две объемные фазы и один поверхностный слой. [37]
Установление равновесия между определенной навеской смолы ( т), высушенной на воздухе, и точно измеренным объемом раствора ( и), общие концентрации металла и лиганда в котором точно известны. При проведении ионного обмена на катионите в растворе может присутствовать фоновый электролит. [38]
Установление зарядового равновесия для термически равновесных и неравновесных процессов протекает по общему механизму. При удалении частиц с поверхности происходит распад первоначальной единой квантовомеханической системы эмиттер - частица на две независимые подсистемы: эмиттер и частица; уходящий от эмиттера поток будет состоять из нейтральных частиц и ионов, положительных и отрицательных. [39]
Установление равновесия коромысла может быть достигнуто путем применения наружного электромагнита при наличии кусочка железа в массивном конце коромысла. Сила тока, идущего в электромагнит для приведения коромысла в равновесие, служит мерой смещения коромысла под действием исследуемого газа. Аналогичное измерение делается для воздуха, и из отношения сил токов определяют удельный вес газа. [40]
Установление металлотропного равновесия ускоряется также в присутствии бромной ртути или нагреванием раствора вещества в четыреххлористом углероде, однако в обоих случаях превращение сопровождается сильным осмолением. [41]
Установление равновесия электронного газа происходит в результате взаимодействия электронов с дефектами решетки, которое сопровождается обменом энергией и импульсом. Такими дефектами являются прежде всего тепловые колебания решетки ( фононы) и примесные атомы. Взаимодействие приводит к рассеянию электронов и установлению беспорядочного движения их в проводнике. [42]
 |
Состав продуктов превращения аммониевых групп анионита АВ-17 ( С1 - после нагревания в спиртах при 453 К. [43] |
Установление равновесия процессов дезаминирования и де-залкилирования аммониевых групп анионита АВ-17 в спиртовых и водно-спиртовых средах [243] свидетельствует об обратимости приведенных выше реакций. Следует отметить, что в водно-спиртовых средах должны протекать те же реакции, что и при нагревании анионитов в воде. [44]
Хорошему установлению равновесия у термометра благоприятствует выделение большого количества кристаллов, а точному определению концентрации, наоборот, - малого. Реальный случай всегда является компромиссным. [45]
Страницы: 1 2 3 4 5