Установление - термодинамическое равновесие
Cтраница 2
Для медленно кристаллизующихся веществ, у которых скорость установления термодинамического равновесия очень мала, отклонение измеренного значения температуры кристаллизации от истинного зависит от скорости теплоотвода. Поэтому Свето-славский [185] предложил определять для таких веществ предельное значение скорости теплоотвода, при которой кривая кристаллизации еще соответствует равновесной кривой. [16]
Повышение температуры в фазе Г требует значительного времени для установления термодинамического равновесия и вызывает релаксационные процессы с высокими значениями постоянных времени. Из-за эффекта пузырьковой релаксации имеет место запаздывание между изменениями давления и объема жидкости. [17]
Так как число молекул ортоводорода и параводорода в ходе установления термодинамического равновесия меняется, мы должны слагаемое Т In N включить во вращательный, а не в поступательный химический потенциал. [18]
Таким образом, либо оказывается невозможным в пределах отведенного времени установление термодинамического равновесия для диссоциации азота: N2 - 2N, но тогда утрачивает смысл и определение теплоты диссоциации N2, либо, как отмечают авторы, необходимо предположить, что более быстрое установление равновесия обеспечивается другой более быстрой реакцией, требующей меньшую энергию активации по сравнению с теплотой диссоциации данной двухатомной молекулы ( N2) [ 96, стр. В настоящее время никаких конкретных предположений, отвечающих этим условиям, не имеется. [19]
Таким образом, либо оказывается невозможным в пределах отведенного времени установление термодинамического равновесия для диссоциации азота: N2 2N, но тогда утрачивает смысл и определение теплоты диссоциации N2, либо, как отмечают авторы, необходимо предположить, что более быстрое установление равновесия обеспечивается другой более быстрой реакцией, требующей меньшую анергию активации по сравнению с теплотой диссоциации данной двухатомной молекулы ( N2) [ 96, стр. В настоящее время никаких конкретных предположений, отвечающих этим условиям, не имеется. [20]
Солюбилизация в белках и мицеллах мыл всегда обратима и характеризуется установлением термодинамического равновесия. Взаимодействия углеводородов с белками и мицел-лярно ассоциированными ПАВ сопровождаются одинаковыми изменениями термодинамических параметров - малыми положительными изменениями энтальпии и увеличением энтропии. Перенос углеводорода в неполярные области мицелл ПАВ и глобулярных белков обусловлен положительными изменениями энтропии [201], равными нескольким десяткам энтропийных единиц. [21]
Такой слой образуется путем перехода ионов из металла в раствор до установления термодинамического равновесия. При этом в металле оказывается избыточное количество электронов. Они и составляют внутреннюю обкладку двойного слоя. Внешней же обкладкой служат гидратированные катионы металла. [22]
В лабораторных условиях проведение работ по вопросу влияния пористой среды на установление термодинамического равновесия связано с известными трудностями. С целью облегчения этих работ было предложено качественно моделировать пористую среду инертным газом - гелием. Соображения, позволяющие проводить качественную параллель между пористой средой и гелием, состоят в следующем. При снятии кривых давления насыщения проба, составленная из бензола и природного газа, дает перелом на кривой, а проба, составленная из бензола и гелия, такого перелома не дает, что служит подтверждением того, что гелий в бензоле совершенно не растворяется. Кроме того, при проведении процессов снижения и повышения давления в системе бензол-гелий петля гистерезиса не образуется. [23]
Конечный размер зерен сорбента и в связи с этим конечность времени установления термодинамического равновесия между двумя фазами определяет такую-неравновесность, благодаря которой происходит дополнительное размывание пятна в направлении движения элюента. [24]
При этом гомогенным мы будем называть такое распределение, которое характеризуется установлением термодинамического равновесия между кристаллом в целом и раствором. [25]
При соприкосновении твердого вещества с растворителем вещество начинает растворяться и по установлении термодинамического равновесия образуется насыщенный раствор. [26]
Нетрудно объяснить появление значительной общей плотности излучения; однако нет условий для установления термодинамического равновесия. [27]
При движении газоконденсатной смеси в пласте и промысловых сооружениях, когда скорость установления термодинамического равновесия между фазами смеси значительно превышает скорость изменения давления или температуры, паровая и жидкая фазы находятся в термодинамическом равновесии. [28]
Ионный обмен - обратимый процесс, приводящий, как правило, к установлению термодинамического равновесия. Это позволяет легко регенерировать иониты после их использования. Катиониты регенерируют слабым раствором кислоты, аниониты - слабым раствором щелочи, слабоосновные аниониты раствором соды. [29]
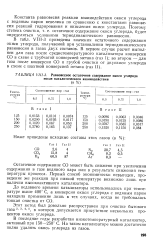 |
Равновесное остаточное содержание окиси углерода после каталитического взаимодействия. [30] |
Страницы: 1 2 3